挥发性有机化合物(VOCs)[1-2]会造成环境污染并严重危害人类健康, 其中, 甲苯在电子、化工、印刷等行业中被广泛用作溶剂或原材料, 是导致白血病甚至致癌的诱因之一[3]。吸附剂通过物理吸附脱除环境中甲苯因其成本低、操作简单而被广泛研究[4⇓-6]。沸石分子筛如5A和13X, 以其优良的吸附容量、价格低廉而被广泛用作吸附剂[7]。例如13X对CO2/N2的选择性高, 是通过变压吸附(PSA)从干燥烟气中捕集CO2最理想的吸附剂之一[8]。由于硅铝比低, 13X具有较强的亲水性, 当有水蒸气存在时, 13X会失去对CO2的吸附能力[9]。因此, 改善材料表面的亲-疏水性对13X等吸附剂有效脱除VOCs具有理论和现实意义。
沸石表面的疏水改性方法较多, 可以通过接枝疏水官能团、后处理提高沸石的硅铝比等措施来提高沸石表面疏水性[10⇓-12]。近年来, 通过在沸石表面涂覆一层介孔硅或高(纯)硅沸石[13⇓⇓⇓⇓⇓⇓-20]来改善沸石的表面特性引起了广泛关注。王强等[14-15]制备了ZSM-5/SBA-15层状结构复合材料, 在外表面沉积一层介孔硅, 使ZSM-5沸石的疏水性能得到显著提高。龙超等[16]制备了NaY@Meso-SiO2核壳复合材料并详细研究了其在潮湿条件下对低浓度VOCs的吸附能力。东北大学杜涛[18]和墨尔本大学Webley[19]等分别制备了13X@SiO2, 并利用氯化三甲基硅烷(TMCS)对制备的核壳结构复合物进行表面硅烷化改性, 进一步提高材料的表面疏水性。表面硅烷化后的样品对CO2的吸附明显提升, 对水的吸附却受到显著抑制[18]。
硅烷偶联剂在高温下易于流失, 利用硅烷偶联剂对沸石表面改性, 在高温条件下使用会降低表面疏水效果; 利用高硅沸石包覆低硅沸石对低硅沸石表面改性, 但微孔孔道延长, 又会限制客体分子扩散。为了提高吸附剂在潮湿环境下对VOCs的吸附能力, 本研究利用正硅酸乙酯在碱性条件下水解, 在13X沸石表面包裹一层介孔硅层, 得到以13X为核, 介孔二氧化硅为壳的核壳复合材料。壳层为介孔纯硅材料, 在提高吸附剂表面疏水性的同时, 壳层的介孔结构还为客体分子传输提供了快速通道。研究还利用甲苯作为探针分子, 研究改性后的13X@SiO2复合材料在不同湿度条件下对VOCs脱除性能。
1 实验方法
1.1 试剂
13X(江西鑫陶科技股份有限公司, BET表面积320 m2/g, 工业品); 氨水、正硅酸乙酯、十六烷基三甲基溴化铵(天津市科密欧化学试剂有限公司); 异丙醇(成都市科隆化学品有限公司)。
1.2 13X@SiO2制备方法
13X@SiO2制备: 先将8 g的13X置于320 mL去离子水中搅拌10 min, 随后超声分散25 min, 待13X分子筛分散均匀, 向上述混合体系中依次加入3.2 g十六烷基三甲基溴化铵(CTABr)、200 mL异丙醇和3.2 mL氨水, 搅拌10 min后加入适量正硅酸乙酯(TEOS), 置于45 ℃水浴锅中恒温搅拌4 h, 然后过滤并用蒸馏水冲洗至中性, 再置于90 ℃烘箱中干燥24 h。最后将干燥样品置于马弗炉中550 ℃焙烧6 h, 得到样品标记为13X@SiO2-v(v代表加入的正硅酸乙酯的体积, mL)。
1.3 表征
采用日本岛津Shimadzu生产的XRD-6000型衍射仪测试X射线衍射(XRD)图谱, Cu Kα射线, 工作电压40 kV, 工作电流30 mA。采用美国Quantachrome仪器公司生产的QUADRASORB SI型吸附仪, 在-196 ℃下获得N2吸附-脱附等温线, 根据BET公式计算样品比表面积(SBET), 采用t-plot法测定微孔体积(Vmicro)和外表面积(Sext), 利用DFT模型(吸附分支)得到中孔体积(Vmeso)和孔径分布图。采用日本岛津FTIR-8400光谱仪分析样品的FT-IR光谱。采用日本Hitachi S4800扫描电子显微镜(SEM)观察样品的晶体尺寸和形貌, 并采用SEM-EDS分析样品表面元素组成。利用日本电子株式会社生产的透射电镜(TEM)JEM-2100F仪分析样品的核壳结构。利用德国KRUSS公司生产的DSA100液滴形状分析仪观察水接触角。
1.4 吸附性能测试
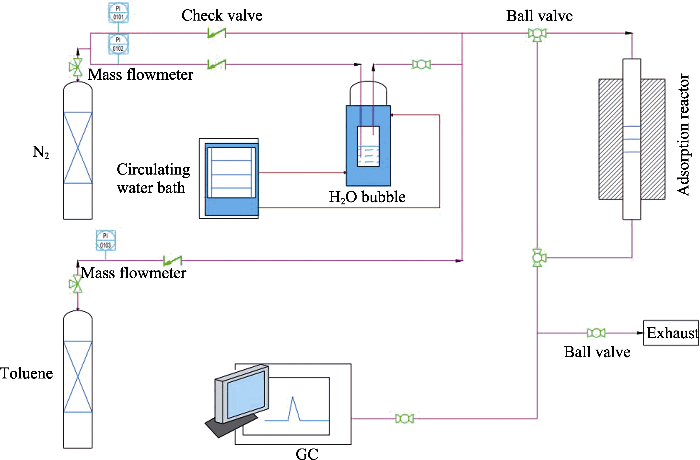
甲苯的吸附穿透实验装置如图S1示意。原料气为1000 μL/L的甲苯与高纯氮的两组分标准气, 出口处的甲苯残留气体浓度用气相色谱仪检测(氢火焰(FID)、HP-PoralPLOT/Q色谱柱), 六通阀自动进样, 进样频率为每次4 min。实验前, 将0.2 g 380~ 830 μm(20~40目)的样品放入反应器中, 50 mL/min氮气流进行吹扫并升温至200 ℃, 维持2 h。活化结束后, 降温至40 ℃, 停止吹扫, 通入甲苯标准气测定样品的吸附突破曲线。由不同类型饱和盐溶液控制甲苯标气的相对湿度[21]。通过积分穿透曲线计算甲苯的平衡吸附容量, 公式如下:
图S1
其中,qe(mg/g)是甲苯的吸附容量, C0(mg/m3)和Ct(mg/m3)分别代表进气和出气浓度, m(g)和ts(min)分别为吸附剂的质量和吸附时间, F(L/min)是气体流量[22]。
2 结果与讨论
图1
图1
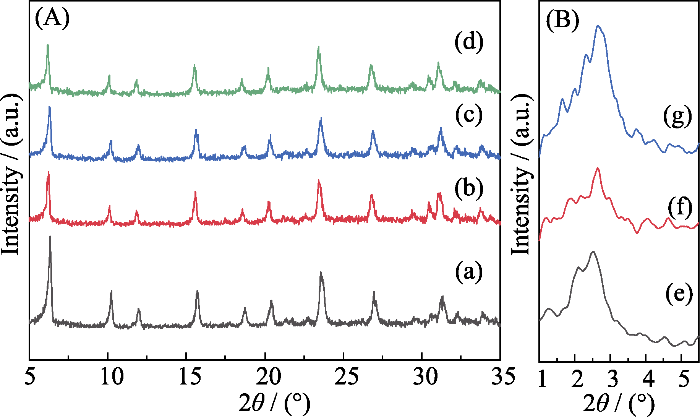
样品(a)13X、(b, e)13X@SiO2-2.2、(c, f)13X@SiO2-2.6和(d, g)13X@SiO2-3.5的XRD图谱
Fig. 1
XRD patterns of the samples of (a) 13X, (b, e) 13X@SiO2-2.2,(c, f) 13X@SiO2-2.6, and (d, g) 13X@SiO2-3.5
(A) Large angle XRD patterns; (B) Small angle XRD patterns
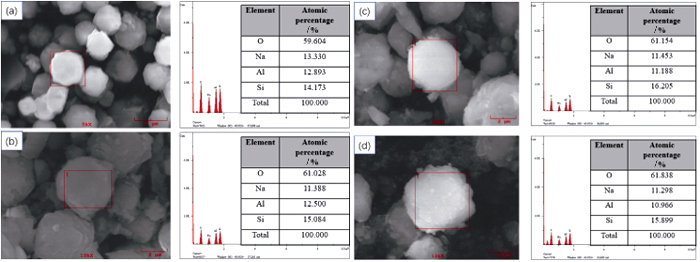
图2为13X及13X@SiO2-v的SEM照片。从图2(A)中可以看出, 13X原样具有“孪生”的八面沸石的形状, 晶体颗粒尺寸约为2~3 μm, 表面粗糙。13X@SiO2-v的外表面较为光滑, 且晶粒尺寸随正硅酸乙酯用量增大而明显增加, 这是由13X外表面沉积了一层二氧化硅(即MCM-41壳层)导致。图2还表明随正硅酸乙酯用量增大, 除13X外表面由粗糙变得光滑外, 样品中还出现了游离的球状小颗粒, 这归因于过量二氧化硅形成的硅微球。且随着正硅酸乙酯用量增大, 硅微球的粒径逐渐增大, 说明13X外表面的MCM-41层的厚度不能无限增厚。 图2(E, F)为样品13X@SiO2-2.2晶粒表层局部破损的SEM照片, 可以看见破损处壳层厚度大约为50 nm。由图S2样品EDS分析结果可见, 13X、13X@SiO2-2.2、13X@SiO2-2.6和13X@SiO2-3.5样品的Si/Al分别为1.10, 1.20, 1.45和1.45, 进一步表明正硅酸乙酯水解后在13X表面沉积了一层介孔二氧化硅。
图2
图2
样品的SEM照片
Fig. 2
SEM images of the samples
(A) 13X; (B, E, F) 13X@SiO2-2.2; (C) 13X@SiO2-2.6; (D) 13X@SiO2-3.5
图S2
图S2
样品的扫描电镜照片及相应的EDS结果
Fig. S2
SEM images and the corresponding EDS results of samples
(A) 13X; (B) 13X@SiO2-2.2; (C) 13X@SiO2-2.6; (D) 13X@SiO2-3.5
图3
图3
样品的TEM照片
Fig. 3
TEM images of the samples
(A, B, E) 13X@SiO2-2.2; (C, D) 13X@SiO2-2.6
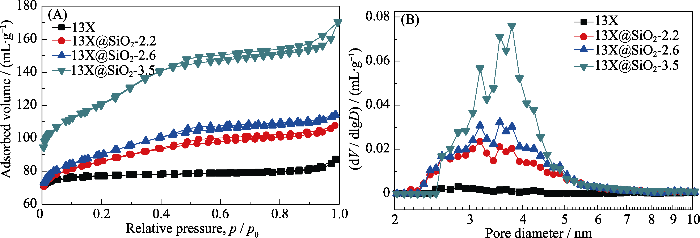
图S3为样品的氮气吸附脱附等温线和对应的DFT模型孔径分布图。13X具有典型的“I”型等温线, 对应孔径分布曲线无明显的介孔结构, 表明13X为纯微孔沸石。沉积二氧化硅样品的等温线为“I+IV”型等温线。随着二氧化硅沉积量增大, 样品13X@SiO2-v在p/p0=0.25~0.45和p/p0=0.45~1.0分别出现滞后环, 且在p/p0=0.25~0.45范围内, 样品的N2吸附量迅速增加, 这归因于13X表面沉积MCM-41壳层的影响。表1为四个样品的氮气吸附脱附数据, 尽管13X样品的比表面较小, 但研究介孔二氧化硅沉积对13X吸附性能尤其是湿VOCs条件下的竞争吸附性能还是有可比性的。与13X原样相比, 随着正硅酸乙酯加入量增大, 13X@SiO2-v系列复合分子筛的比表面积和外表面积呈逐渐增大趋势, 而微孔面积和微孔容积逐渐减小。从图S3(B)孔径分布曲线可以看出, 13X@SiO2-v系列样品中存在均匀的3~5 nm介孔结构。
图S3
图S3
样品的(A)氮气吸附脱附等温曲线与(B)DFT模型孔径分布图
Fig. S3
(A) Nitrogen adsorption-desorption isothermal curves and (B) the corresponding pore size distributions decided by a DFT model of samples
表1 样品的比表面积及孔结构参数
Table 1
| Sample | SBET/(m2·g-1) | Sext/(m2·g-1) | Smic/(m2·g-1) | Vmic/(cm3·g-1) | Vmes/(cm3·g-1) |
|---|---|---|---|---|---|
| 13X | 314 | 14 | 299 | 0.11 | 0.02 |
| 13X@SiO2-2.2 | 324 | 95 | 229 | 0.09 | 0.07 |
| 13X@SiO2-2.6 | 337 | 130 | 207 | 0.08 | 0.09 |
| 13X@SiO2-3.5 | 444 | 259 | 184 | 0.07 | 0.18 |
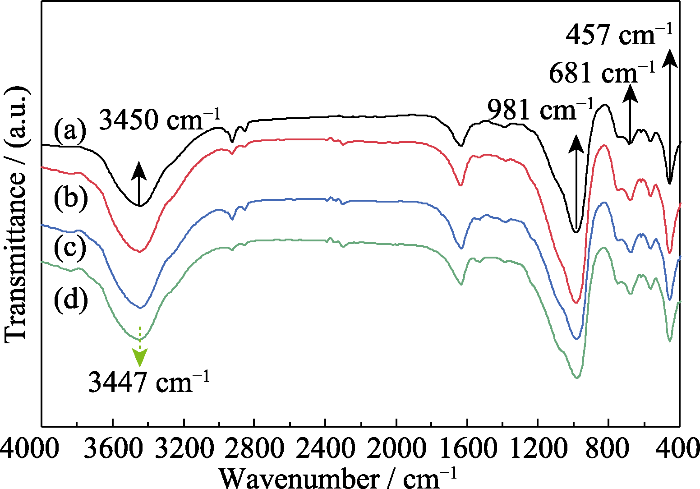
图S4为13X@SiO2-v与13X沸石的红外光谱图。由图可见13X沸石在3450 cm-1附近处的红外吸收峰归属于Si-OH的伸缩振动吸收峰, 457、681和981 cm-1处的红外吸收峰归属于13X沸石内部的铝氧四面体和硅氧四面体的振动峰。图S4还表明经MCM-41包裹后, 样品的Si-OH伸缩振动吸收峰向低波数偏移至3447 cm-1处, 这是由材料的疏水性增加, 与水的结合变弱引起[25]。水接触角大小可以直接反映材料外表面的疏水性强弱。如图S5所示, 水滴在13X沸石表面没有凝结, 因为水一接触13X表面就被吸附, 说明13X具有很强的亲水性。13X@SiO2-v系列核壳复合材料对水滴没有立即吸收, 虽然核壳材料表面水接触角都小于90°[12,14,16,22], 但表面水滴均表现出一定程度的凝聚。上述结果说明, 与13X沸石相比, 13X@SiO2-v系列核壳复合材料的疏水性得到一定程度的提高, 其中13X@SiO2-2.6的水接触角最大, 达到17.8°, 13X@SiO2-2.2和13X@SiO2-3.5的相近但比13X@SiO2-2.6接触角小。
图S4
图S4
样品的红外光谱
Fig. S4
FT-IR spectra of the sample
(a) 13X; (b) 13X@SiO2-2.2; (C) 13X@SiO2-2.6; (D) 13X@SiO2-3.5
图S5
图S5
不同改性沸石的水接触角测量照片
Fig. S5
Images of water droplets on the surfaces of different samples
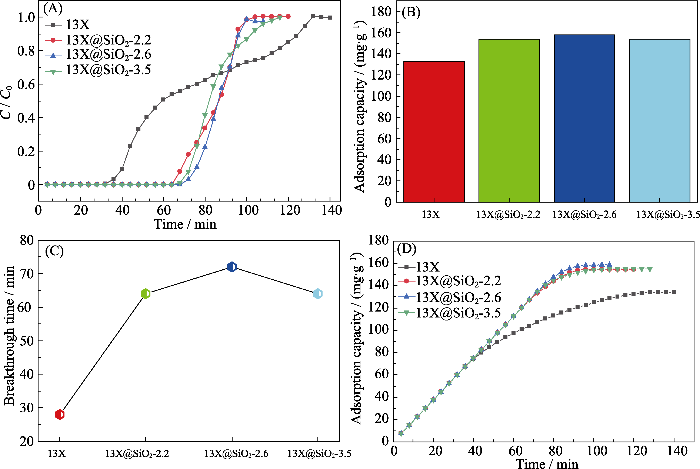
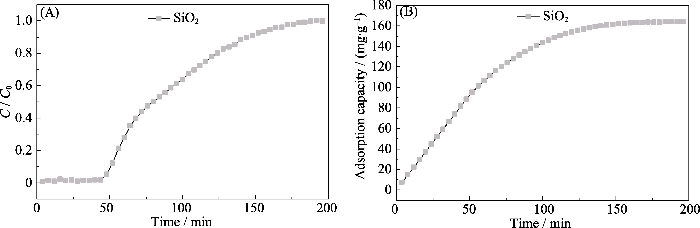
当吸附质中不含水蒸气时, 对甲苯吸附穿透曲线和累积吸附量图如图4和图S6所示, 纯介孔二氧化硅的突破时间为44 min, 饱和吸附量为163 mg/g,优于干条件下13X的饱和吸附量(134 mg/g); 13X@SiO2-v比13X原样具有更长的穿透时间(尾气中探测到明显吸附质时间)和更多甲苯的吸附量。图4(B, D)表明13X@SiO2-2.2、13X@SiO2-2.6、13X@SiO2-3.5的饱和吸附容量分别为154、159和155 mg/g, 比13X(134 mg/g)分别提高了16%、18%、15.8%, 这归因于壳层的影响, 即增加的吸附量应该是壳层增加和13X减少共同作用的结果。从突破时间来看, 甲苯在上述三个样品的突破时间分别为64、72、64 min, 远比13X的(28 min)大(如图4(C)), 表明在相同环境下复合材料比13X对甲苯具有更好的去除效果。对13X@SiO2-v核壳样品而言, 其比表面积和外比表面积的提升, 增大了吸附剂与甲苯之间的范德华作用力[26]。
图4
图4
干条件下不同吸附剂对甲苯的吸附实验
Fig. 4
Adsorption of toluene on the different adsorbents under dry condition
(A) Adsorption breakthrough curves; (B) Saturated adsorption capacity; (C) Comparison of the breakthrough times; (D) Cumulative adsorption capacity of different adsorbents
图S6
图S6
SiO2在干条件下对甲苯的(A)吸附穿透曲线和(B)累积吸附量
Fig. S6
(A) Toluene adsorption breakthrough curves and (B) cumulative toluene adsorption capacity of SiO2 under dry condition
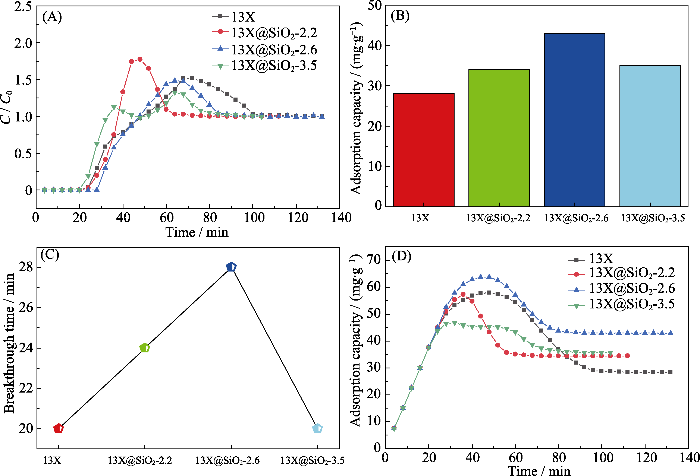
在30%相对湿度下, 所有样品的甲苯吸附量显著下降,穿透时间显著缩短, 这归因于混合气体中的水分子与甲苯竞争吸附剂中的吸附位, 降低了对甲苯的吸附量。对比图4(B)和图5(B)可见, 与核/壳复合样品相比, 达到吸附平衡时13X对苯的吸附量下降更加明显。13X由于硅/铝比小、表面亲水的特性, 造成在水汽-甲苯对吸附位的竞争过程中, 甲苯处于劣势。与干条件相比, 在30%相对湿度下, 13X沸石对甲苯吸附量下降了79%; 由图5(B)还可知, 30%相对湿度环境下, 13X、13X@SiO2-2.2、13X@SiO2-2.6、13X@SiO2-3.5对甲苯的吸附容量分别为28、34、43和35 mg/g, 其中13X@SiO2-2.2和13X@SiO2-2.6比13X分别提高21%和53%。三个复合样品中13X@SiO2-2.6的饱和吸附量最高, 这是因为它具有最好的表面疏水特性(图S5)。
图5
图5
不同吸附剂在相对湿度30%条件下对甲苯的吸附实验
Fig. 5
Adsorption of toluene on the different adsorbents under 30% relative humid conditions
(A) Adsorption breakthrough curves; (B) Saturated adsorption capacity; (C) Comparison of the breakthrough time; (D) Cumulative adsorption capacities of different adsorbents of toluene
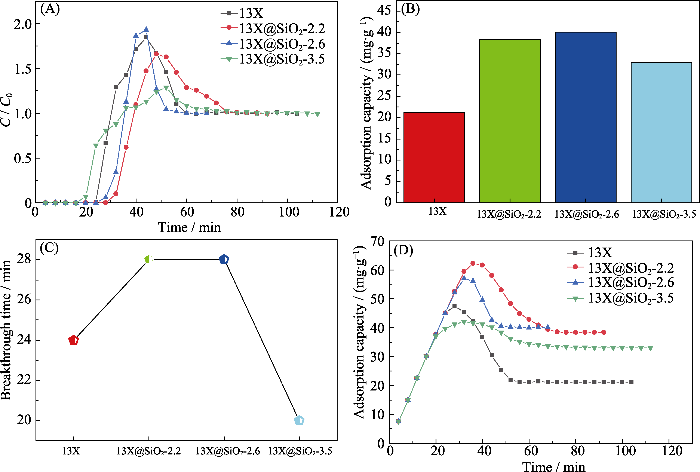
50%相对湿度条件(图6)与30%相对湿度条件具有相似的吸附结果。13X、13X@SiO2-2.2、13X@SiO2-2.6和13X@SiO2-3.5的达峰时间分别为20、24、28、20 min, 三个核壳样品对甲苯的吸附容量分别为38、40和32 mg/g, 分别比13X(21 mg/g)对甲苯的吸附量提高了80%, 90%和52%。上述结果表明, 包裹SiO2层改善了沸石的疏水性, 在湿度更高的极端条件下, 壳层SiO2也起到更优异的疏水作用, 说明壳层SiO2减少了对水分子的吸附, 增加了对甲苯的亲和力, 提高了对甲苯的吸附能力。
图6
图6
不同吸附剂在相对湿度50%条件下对甲苯的吸附实验
Fig. 6
Adsorption of toluene on the different adsorbents under 50% relative humid conditions
(A) Adsorption breakthrough curves; (B) Saturated adsorption capacity; (C) Comparison of the breakthrough time; (D) Cumulative adsorption capacity of different adsorbents of toluene
图S7
图S7
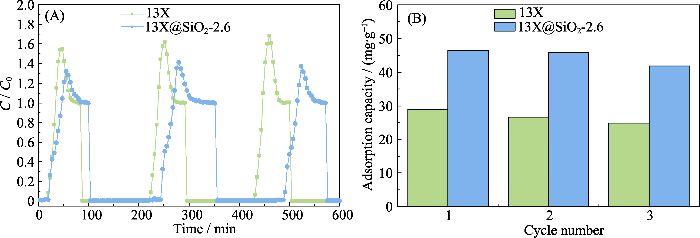
50% RH下, 13X和13X@SiO2-2.6的(A)三次吸附-脱附循环吸附穿透曲线与(B)饱和吸附量变化曲线
Fig. S7
(A) Adsorption of toluene on different adsorbents with triple adsorption-desorption cycle. Adsorption penetration curve and (B) saturated adsorption capacity under 50% relative humid conditions
3 结论
通过控制正硅酸乙酯的水解在13X表面沉积了一层介孔二氧化硅, 并得到了具有核壳结构的13X@SiO2复合分子筛:
1) 在干条件下13X@SiO2-v复合物比13X具有更长的穿透时间和更多甲苯的吸附量, 其中13X@SiO2-2.6比13X沸石对甲苯吸附量提高了18%;
2) 在30%相对湿度下, 所有样品的甲苯吸附量和穿透时间都显著下降, 归因于混合气体中水分子和甲苯之间的竞争吸附, 从而降低对甲苯的吸附量, 其中13X@SiO2-2.2和13X@SiO2-2.6分别比13X沸石提高21%和53%;
3) 在50%相对湿度条件下, 13X@SiO2-2.2、13X@SiO2-2.6和13X@SiO2-3.5对甲苯的吸附容量分别为38、40和32 mg/g, 分别比13X(21 mg/g)对甲苯的吸附量提高了80%, 90%和52%。
4) 包裹SiO2层改善了沸石的疏水性, 在湿度更高的极端条件下, 壳层SiO2也起到了更优异的疏水作用, 减少了对水分子的吸附, 增加了对甲苯的亲和力, 从而提高了对甲苯的吸附能力。
补充材料
本文相关补充材料可登陆
参考文献
Catalytic oxidation of volatile organic compounds (VOCs)-a review
Catalytic combustion of VOCs on non-noble metal catalysts
Adsorptive removal of toluene and dichloromethane from humid exhaust on MFI, BEA and FAU zeolites: an experimental and theoretical study
Enhanced hydrophobic UiO-66 (University of Oslo 66) metal-organic framework with high capacity and selectivity for toluene capture from high humid air
Design of dual functional adsorbent/ catalyst system for the control of VOC’s by using metal-loaded hydrophobic Y-zeolites
Experimental and modeled results describing the adsorption of toluene onto activated carbon
Polyethylenimine- modified zeolite 13X for CO2 capture: adsorption and kinetic studies
An experimental adsorbent screening study for CO2 removal from N2
Cosorption characteristics of solid adsorbents
Engineering surface functional groups on mesoporous silica: towards a humidity-resistant hydrophobic adsorbent
Adsorption of tetrachloroethylene (PCE) in gas phase on zeolites of faujasite type: Influence of water vapour and of Si/Al ratio
Prepared hydrophobic Y zeolite for adsorbing toluene in humid environment
Core-shell composites of USY@mesosilica: synthesis and application in cracking heavy molecules with high liquid yield
Hierarchical structure ZSM-5/ SBA-15 composite with improved hydrophobicity for adsorption- desorption behavior of toluene
Synthesis of ZSM-5/siliceous zeolite composites for improvement of hydrophobic adsorption of volatile organic compounds
In this research, we investigated the hydrophobicity and dynamic adsorption-desorption behaviors of volatile organic compounds (VOCs) by applying different optimized coating dosage (25, 50, and 75%) on designed novel ZSM-5/MCM-41 and ZSM-5/Silicalite-1 hierarchical composites. The relatively large specific surface area and pore volume of adsorbents ZSM-5/MCM-41 and ZSM-5/Silicalite-1 composites with excellent stability were affirmed by XRD, FTIR, BET, SEM, and water contact angle analyses. Regarding, toluene adsorption-desorption investigation, ZSM-5/MCM-41 composite lead a longer stable toluene breakthrough time no matter under dry or 50% humid conditions. However, under different loading dosage condition, the breakthrough time of 75% coating ratio was the longest, which was 1.6 times as long as that of pure ZSM-5 under wet adsorption. Meanwhile, the complete elimination of toluene for ZSM-5/MCM-41-75% was done by largest desorption peak area and the lowest desorption temperature of 101.9°C, while, the largest contact angle of ZSM-5/MCM-41-75% was 17.0° higher than pure ZSM-5 zeolite. Therefore, we believe that the present hydrophobic sorbent will provide new insight with great research potential for removing low concentration of VOCs at industrial scale.
Enhancing adsorption capacities of low-concentration VOCs under humid conditions using NaY@meso-SiO2 core-shell composite
High water tolerance of a core-shell-structured Zeolite for CO2adsorptive separation under wet conditions
Preparation of hydrophobic zeolite 13X@SiO2and their adsorption properties of CO2and H2O
Synthesis of hydrophobic zeolite X@SiO2 core-shell composites
Microporous zeolite@vertically aligned Mg-Al layered double hydroxide core@shell structures with improved hydrophobicity and toluene adsorption capacity under wet conditions
Introduction to the standard relative humidity table for saturated salt solutions (international recommendation)
Core-shell structured Y zeolite/ hydrophobic organic polymer with improved toluene adsorption capacity under dry and wet conditions
ZSM-5@MCM-41 composite porous materials with a core-shell structure: Adjustment of mesoporous orientation basing on interfacial electrostatic interactions and their application in selective aromatics transport
One-pot synthesis of SiO2@SiO2 core-shell microspheres with controllable mesopore size as a new stationary phase for fast HPLC separation of alkyl benzenes and β-agonists
Metal-organic frameworks for the adsorption of gaseous toluene under ambient temperature and pressure
Competing adsorption of toluene and water on various zeolites
Post synthetic modification of zeolite internal surface for sustainable capture of volatile organic compounds under humid conditions
Rapid cycling thermal swing adsorption apparatus: commissioning and data analyses for water adsorption of zeolites 4A and 13X over 2000 cycles
Insights into the hydrothermal stability of zeolite 13X