能源和环境是当今人类生存与社会发展所必须应对的两个重大问题。随着煤炭、石油等化石资源的枯竭和环境的日益恶化, 发展太阳能、风能和水能等可再生能源已经成为全球性趋势。为了将其安全高效地整合到电网中, 大规模储能设备应运而 生[1,2]。在各种储能技术中, 电化学储能以其灵活便捷、能量转换效率高、成本低、设备维护简单等优点而被认为是最有发展前景的储能技术。锂离子电池具有比容量高、循环寿命长、工作电压高等特点, 被广泛应用于便携式电子产品[3,4], 同时也被认为是电动汽车的最佳选择。尽管锂离子电池取得了巨大成功, 但其使用的有机电解质毒性高, 使用过程中存在易燃风险, 并且地壳中锂资源有限、分布不均匀, 成本较高。这些因素都限制了它在大规模储能方面的应用。因此, 人们开始将注意力转移到水系电池, 利用水系电解液代替有机电解液的电池体系, 可进一步降低电池的生产成本、提高电池的安全性。水系电解液的离子电导率比有机电解液高2个数量级, 因而水系电池通常具有更高的功率密度[5,6]。目前已发展的水系电池有:水系锂离子电池[7,8,9,10]、钠离子电池[11,12,13]、镁离子电池[14]、锌离子电池[15,16,17]和水系混合离子电池[18,19,20,21,22]。这些水系电池在实际应用中安全无风险且价格低廉, 在大规模储能方面具有广阔的发展前景。
本研究以Na4Fe(CN)6作为单一铁源, 通过简单的水热法合成出高质量的Fe4[Fe(CN)6]3(HQ-FeHCF)纳米材料。另外用传统的方法合成出低质量的Fe4[Fe(CN)6]3(LQ-FeHCF)纳米材料作为对比, 研究HQ-FeHCF和LQ-FeHCF的结构形貌特征和电化学性能。最后, 以HQ-FeHCF为正极, NaTi2(PO4)3为负极, NaClO4-H2O-聚乙二醇(PEG)为电解液, 组装成水系钠离子全电池。
1 实验方法
1.1 仪器与试剂
采用输力强电化学工作站(Solartron 1470E multi- channel potentiostats)进行恒流充放电测试和循环伏安测试。XRD采用德国Bruker D8 advance-X射线衍射仪, Cu Kα靶, 管电压为40 kV, 管电流为40 mA, 扫描速率为7(°)/min, 2θ角范围为10°~60°。使用日本日立S-4800扫描电子显微镜(SEM)观察样品的形貌和颗粒大小, 发射电压为20 kV。使用日本电子株式会社JEM2100型透射电子显微镜(TEM)来观察材料内部显微结构以及晶体缺陷, 并分析材料元素成分。
实验所用的化学试剂:盐酸、聚乙烯吡咯烷酮K-30、十水合亚铁氰化钠、六水合三氯化铁均为国药集团化学试剂有限公司生产, 分析纯。
1.2 电极材料的制备
室温下, 将4 g聚乙烯吡咯烷酮K-30(PVP)和0.126 g十水合亚铁氰化钠加入到50 mL pH=0.8的盐酸水溶液中, 搅拌1 h, 完全溶解后溶液呈黄色。然后将搅拌均匀的溶液放入80 ℃烘箱中保温12 h。将降到室温的溶液进行离心分离得到沉淀并用去离子水洗涤, 重复4次后, 在80 ℃烘箱中干燥8 h即得到HQ-FeHCF样品。
将2.7 g六水合三氯化铁和3.6 g十水合亚铁氰化钠分别加入到100 mL去离子水中, 60 ℃下搅拌至两种溶液完全溶解, 然后将六水合三氯化铁盐溶液加入十水合亚铁氰化钠盐溶液中, 生成大量深蓝色沉淀。60 ℃下保温1 h后, 将溶液进行离心分离得到沉淀, 并用去离子水洗涤, 重复4次后, 在80 ℃烘箱中干燥8 h, 即得到LQ-FeHCF样品。
1.3 材料的电化学测试
将所制得的电极材料按照m(活性物质):m(乙炔黑):m(聚偏氟乙烯(PVDF))=75:15:10的比例进行混合, 加入适量N-甲基吡咯烷酮(NMP)搅拌8 h, 然后将搅拌均匀的浆料涂抹在直径约为1.3 cm的圆形钛网上, 在80 ℃烘箱中烘干12 h, 然后用压片机在 10 MPa的压力下压成薄片, 制成工作电极。以铂丝为对电极, 氯化银为参比电极, 组装成三电极体系, 测试了HQ-FeHCF的充放电平台、倍率性能和循环稳定性。以直径为1.3 cm的HQ-FeHCF极片为正极(活性物质载量1.14 mg), NaTi2(PO4)3极片为负极(活性物质载量2.73 mg), 组成全电池进行恒流充放电性能测试, 电池体系恒流充放电电压区间为0~2 V。电极放电容量和电池能量密度只按照活性物质的质量计算。电解液采用NaClO4+H2O+Polyethylene glycol(PEG)体系。
2 结果与讨论
2.1 材料的结构表征
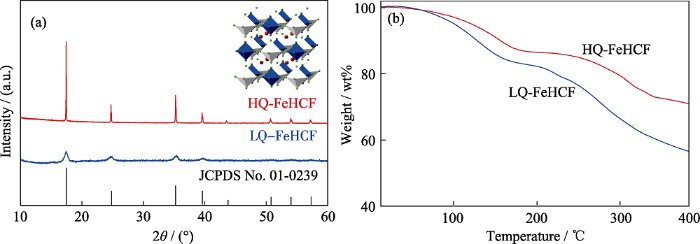
图1(a)为HQ-FeHCF和LQ-FeHCF的XRD图谱, 从图中可以看出, HQ-FeHCF的所有衍射峰均与JCPDS NO. 01-0239卡片相符, 说明所合成的HQ-FeHCF具有面心立方(fcc)结构, 属于fm-3m空间点群, a=b=c=0.51 nm, α=β=γ=90°。其中没有任何杂峰出现, 说明所合成的HQ-FeHCF纯度高, 其锐利的特征峰也说明通过添加PVP缓慢合成的HQ-FeHCF纳米材料结晶性优异, 具有典型的Fe4[Fe(CN)6]3晶体结构[34]。通过快速沉淀所制得的LQ-FeHCF衍射峰不尖镜, 表明其结晶性差。图1(a)中右上角插图为HQ-FeHCF的晶胞结构示意图, 它是由开放型三维框架组成, Fe1与六个氮原子相连接, Fe2被与氰化物配位的碳原子八面体包围。此开放框架结构中间留有大的间隙位点, 为Na+的嵌入/脱出提供了足够大的空间[31, 35]。为了确定所合成材料中结晶水的含量, 对HQ-FeHCF和LQ-FeHCF进行了热重分析测试, 在N2气氛下, 以10 ℃/min的加热速率测得的结果如图1(b)所示。30~200 ℃阶段的失重, 对应着结晶水的去除; 200~400 ℃阶段的失重, 对应着[Fe(CN)6]的分解。从图1(b)中可看出HQ- FeHCF结晶水的含量为13%, LQ-FeHCF结晶水的含量为18%。HQ-FeHCF比LQ-FeHCF含有的结晶水更少, 这也表明HQ-FeHCF比LQ-FeHCF的[Fe(CN)6]空位缺陷更少[36]。为进一步精确测试材料中[Fe(CN)6]空位缺陷的含量, 对HQ-FeHCF和LQ-FeHCF进行了XRD精修处理, 如表1、表2所示。在HQ-FeHCF中, Fe2/Fe1原子比为0.91, 表明其存在9%的[Fe(CN)6]空位缺陷; 在LQ-FeHCF中, Fe2/Fe1原子比为0.74, 表明[Fe(CN)6]空位缺陷含量为26%。
图1
图1
HQ-FeHCF和LQ-FeHCF的(a)XRD图谱和(b)TG曲线, (a)中插图为HQ-FeHCF晶胞结构示意图
Fig. 1
(a) XRD patterns and (b)TG curves of HQ-FeHCF and LQ-FeHCF with inset in (a) showing crystal structure of HQ-FeHCF
表1 HQ-FeHCF的XRD精修数据
Table 1
| Atom | Wyckoff position | x | y | z | Site occupancy |
|---|---|---|---|---|---|
| Fe1 | 4a | 0.0000 | 0 | 0 | 0.9790 |
| Fe2 | 4b | 0.5000 | 0 | 0 | 0.8901 |
| C | 24e | 0.2024 | 0 | 0 | 0.9771 |
| N | 24e | 0.2988 | 0 | 0 | 0.9771 |
表2 LQ-FeHCF的XRD精修数据
Table 2
| Atom | Wyckoff position | x | y | z | Site occupancy |
|---|---|---|---|---|---|
| Fe1 | 4a | 0.0000 | 0 | 0 | 0.8458 |
| Fe2 | 4b | 0.5000 | 0 | 0 | 0.6262 |
| C | 24e | 0.2260 | 0 | 0 | 0.8420 |
| N | 24e | 0.3275 | 0 | 0 | 0.8420 |
图2(a~b)为HQ-FeHCF在不同放大倍数下的SEM照片, 可清晰看出HQ-FeHCF为边长约500 nm的正方体结构, 正方体表面规则完整且样品颗粒分散良好、尺寸均匀、无严重堆积现象。图2(c~d)为LQ-FeHCF在不同放大倍数下的SEM照片, 可看出LQ-FeHCF呈不规则颗粒状。这是因为快速的沉淀过程使得LQ-FeHCF不具有完整规则的结构形貌, 且存在大量无序的[Fe(CN)6]空位缺陷和结晶水, 也会导致LQ-FeHCF的电化学性能不佳。为进一步观察HQ-FeHCF和LQ-FeHCF的微观形貌, 对材料进行了TEM表征。如图3(a)所示, 每个HQ-FeHCF纳米立方颗粒边缘光滑且形状完整, 无明显缺陷, 也说明所合成的HQ-FeHCF结晶性好, 质量高。如图3(b) 所示, LQ-FeHCF颗粒大小不一且无规则的结构特征, 这与图2中LQ-FeHCF的SEM照片相吻合,表明LQ-FeHCF结晶性差、质量低、缺陷多。
图2
图2
(a~b)HQ-FeHCF和(c~d)LQ-FeHCF的SEM照片
Fig. 2
SEM images of (a-b) HQ-FeHCF and (c-d) LQ-FeHCF
图3
图3
(a)HQ-FeHCF和(b)LQ-FeHCF的TEM照片
Fig. 3
TEM images of (a) HQ-FeHCF and (b) LQ-FeHCF
2.2 电化学性能测试
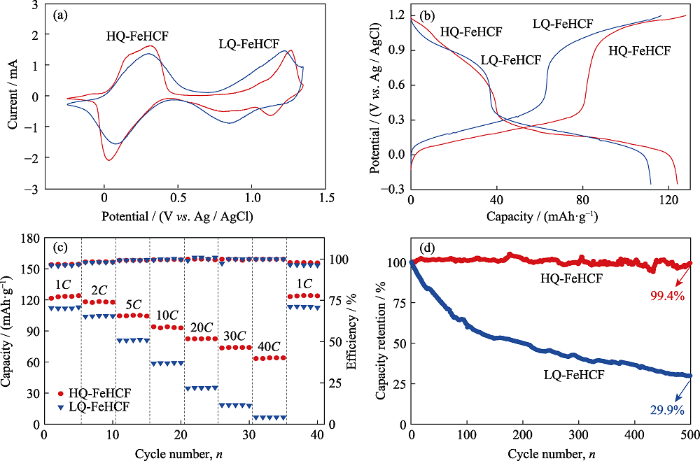
首先, 采用三电极体系测试了HQ-FeHCF和LQ-FeHCF在Na-H2O-PEG电解液中的电化学性能。图4(a)为HQ-FeHCF和LQ-FeHCF在Na-H2O-PEG电解液中的循环伏安曲线, 扫描速率为1 mV·s-1。从图中可以清晰地观察到HQ-FeHCF出现两对独立的氧化还原峰, 表明发生了两次氧化还原反应, 对应了两个Na+的可逆嵌入/脱出[37]。第一对氧化还原峰出现在0.03和0.28 V, 对应于与碳原子相连接的高自旋FeⅢ/FeⅡ离子的还原和氧化, 第二对氧化还原峰出现在1.12和1.26 V, 对应于与氮原子键合的低自旋FeⅢ/FeⅡ离子的还原和氧化[35, 38]。在相同扫速下, LQ-FeHCF与HQ-FeHCF的CV曲线相类似。图4(b)为HQ-FeHCF和LQ-FeHCF在1C (1C= 120 mA·g-1)倍率下的恒流充放电曲线。从图中可明显看出, HQ-FeHCF在充放电过程中各出现2个电压平台, 表明Na+的嵌入/脱出是分两步完成的, 这与图4(a)中出现的两对氧化还原峰相对应。LQ-FeHCF显示出与HQ-FeHCF相类似的充放电曲线, 但其放电容量明显小于HQ-FeHCF。图4(c)是HQ-FeHCF和LQ-FeHCF的倍率性能, 从图中可看出HQ-FeHCF在1C、2C、5C、10C、20C、30C和40C倍率下的比容量分别为124、118、105、94、83、74和63 mAh·g-1, 值得注意的是, 当再次回到1C时, 容量又恢复到124 mAh·g-1, 显示出了极佳的倍率性能。HQ-FeHCF之所以有如此好的倍率性能, 有两个原因: 第一, 采用本文中的方法所合成出的HQ-FeHCF材料质量高、空位缺陷少, 从而确保了Na+的高效传输; 第二, 材料的大通道结构缩短了Na+的传输路径。此外, 通过添加PVP缓慢合成的HQ-FeHCF结构十分稳定, 大倍率下的充放电循环也没有使HQ-FeHCF的结构坍塌从而出现电化学性能下降。LQ-FeHCF在1C、2C、5C、10C、20C、30C和40C倍率下的比容量分别为112、104、81、59、35、18和7 mAh·g-1, 整体倍率性能较之HQ- FeHCF要差, 特别是在大倍率下, 差距尤为明显, 这是因为LQ-FeHCF没有稳定的结构, 且其晶体内存在大量的[Fe(CN)6]空位缺陷和结晶水, 阻碍了Na+的脱嵌从而导致LQ-FeHCF在大倍率下比容量极低。
图4
图4
(a)HQ-FeHCF和LQ-FeHCF在Na-H2O-PEG电解液中以1 mV·s-1的扫速测得的循环伏安曲线; (b)HQ-FeHCF和LQ-FeHCF在1C倍率下的充放电曲线; (c)HQ-FeHCF和LQ-FeHCF的倍率性能; (d)HQ-FeHCF和LQ-FeHCF的循环性能
Fig. 4
(a) Cyclic voltammogram (CV) curves of HQ-FeHCF and LQ-FeHCF at the sweep rate of 1 mV·s-1 in the electrolyte of Na-H2O-PEG; (b) Charge and discharge curves of HQ-FeHCF and LQ-FeHCF at 1C; (c) Rate performance of HQ-FeHCF and LQ-FeHCF; (d) Cycling performance of HQ-FeHCF and LQ-FeHCF
循环稳定性是水系钠离子电池在实际应用中的一个重要参数。5C倍率下HQ-FeHCF和LQ-FeHCF的循环性能如图4(d)所示。LQ-FeHCF在第一个循环中的放电容量为87 mAh·g-1, 但是其容量随着循环次数的增加而快速下降, 100个循环后, 其容量保持率为61%, 500个循环后, 其容量只有26 mAh·g-1, 对应的容量保持率为29.9%。HQ-FeHCF则显示出了极其优异的循环稳定性, 100个循环后, HQ-FeHCF的容量没有明显的下降, 维持着100%的容量保持率, 直到第500次循环, 容量保持率仍高达99.4%。值得注意的是, HQ-FeHCF的循环稳定性不仅远超LQ-FeHCF, 甚至优于文献[30, 38]报道的有机系FeHCF阴极材料。
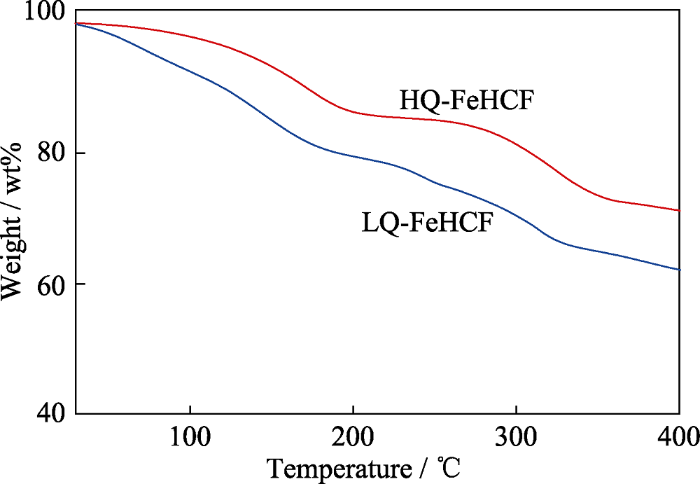
为进一步验证HQ-FeHCF在Na-H2O-PEG电解液中的稳定性, 分别将循环100圈和500圈后的极片进行SEM观察。如图5所示, 图5(a~b)为HQ-FeHCF在Na-H2O-PEG电解液中5C恒流充放电100次后的SEM照片, 从图中可清晰看出, 每个HQ-FeHCF纳米立方体颗粒都保持了高度完整性, 几乎没有任何结构的破坏, 颗粒表面无缺陷产生。图5(c~d)为HQ-FeHCF在Na-H2O-PEG电解液中5C恒流充放电500次后的SEM照片, 每个HQ-FeHCF纳米立方体颗粒同样保持高度完整, 无任何结构变形或坍塌。将循环500次后的极片进行TG测试, 如图6所示, HQ-FeHCF结晶水的含量为13%, 较循环前无明显变化; LQ-FeHCF结晶水的含量为20%, 较循环前增加了2%。
图5
图5
循环(a~b) 100次和(c~d) 500次后 HQ-FeHCF的SEM照片
Fig. 5
SEM images of HQ-FeHCF after (a-b)100 and (c-d) 500 cycles
图6
图6
循环500次后HQ-FeHCF和LQ-FeHCF的TG曲线
Fig. 6
TG curves of HQ-FeHCF and LQ-FeHCF after 500 cycles
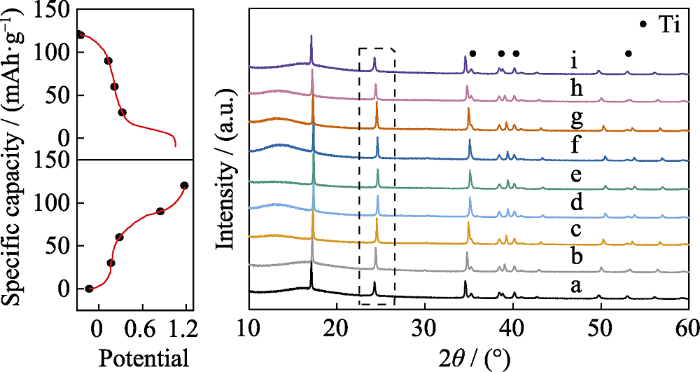
采用非原位XRD技术研究了HQ-FeHCF材料在电化学反应过程中的相变机制。图7是在不同充放电状态下材料的XRD图谱, a~e为充电过程, f~i为放电过程, 其中圆点处标记的为Ti的衍射峰。以虚线框中的一组衍射峰为例, 从图中可明显看出a~e过程中XRD衍射峰向2θ增大方向偏移,由24.3°增大到24.6°, 这是因为充电过程Na+从HQ-FeHCF中脱出从而引起晶格收缩。此过程中的晶胞体积变化约为8.1%。f~i过程中XRD衍射峰向2θ减小方向偏移, 又重新回到24.3°, 这是因为在放电过程中Na+又重新嵌入HQ-FeHCF从而引起晶格膨胀。值得注意的是, a和i衍射峰的位置高度重合, 表明Na+在HQ-FeHCF材料中的脱嵌是高度可逆的,并且Na+的可逆脱嵌并不会破坏材料的晶体结构, 也说明HQ-FeHCF在Na-H2O-PEG电解液中的稳定性高。
图7
图7
不同荷电状态下HQ-FeHCF的XRD图谱
Fig. 7
Ex situ XRD patterns of HQ-FeHCF material at various states of charge and discharge
NASICON型NaTi2(PO4)3具有适合钠离子扩散的开放型三维结构, 因此NaTi2(PO4)3既可以用作有机系钠离子电池电极材料, 也可以用作水系钠离子电池电极材料。通过先前的方法制得NaTi2(PO4)3, 采用循环伏安法(CV)和恒流充放电研究了其在Na-H2O-PEG电解液中的电化学性质。图8(a)显示了NaTi2(PO4)3在1 mV·s-1扫速下的CV曲线, 在-0.64和-0.79 V(vs. Ag / AgCl)处有一对尖锐的氧化还原峰, 对应着Na+的嵌入/脱出, 并伴随着Ti3+和Ti4+之间的可逆转换。NaTi2(PO4)3的电压分布如图8(b) 所示, -0.69 V(vs. Ag/AgCl)处平坦的放电平台表明NaTi2(PO4)3是良好的水系钠离子电池负极材料。
图8
图8
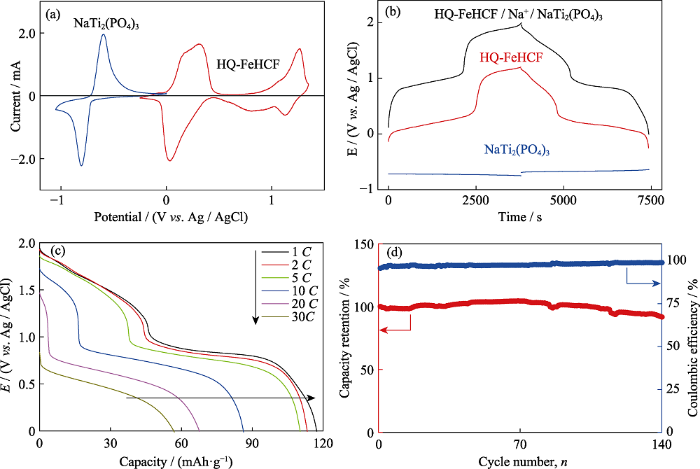
(a)HQ-FeHCF和NaTi2(PO4)在Na-H2O-PEG电解液中以1 mV·s-1的扫速测得的循环伏安曲线; (b)1C倍率下正极、负极和全电池的衡流充放电曲线;全电池的(c)倍率性能和(d)循环性能
Fig. 8
(a) Cyclic voltammogram (CV) curves of HQ-FeHCF and NaTi2(PO4) at the sweep rate of 1 mV·s-1 in the electrolyte of Na-H2O-PEG; (b) Galvanostatic charge-discharge profiles at 1C for full cell, cathode, and anodein the electrolyte of Na-H2O-PEG; (c) Rate performance and (d) cycling performance of full cell
基于HQ-FeHCF和NaTi2(PO4)3良好的电化学性能, 组装了以HQ-FeHCF为正极, NaTi2(PO4)3为负极, NaClO4-H2O-PEG为电解液的水系钠离子全电池。图8(b)显示了正极、负极和全电池在1C倍率下的电压曲线, 从图中可看出全电池的工作电压高达1.9 V。高的工作电压有利于提高全电池的能量密度, 基于活性物质的质量计算所得到的全电池能量密度高达126 Wh·kg-1, 超越了多数之前所报道的以锰氧化物、磷酸盐以及普鲁士蓝为正极材料的水系钠离子全电池能量密度, 具体对比如表3所示。如图8(c)所示, 在1C、2C、5C、10C、20C和30C的倍率下, 全电池的容量分别为117、113、110、86、68和57 mAh·g-1, 显示出优异的倍率性能。图8(d)为5C倍率下全电池的循环性能。在前70次循环中, 全电池的容量略有增加, 库伦效率从第一圈的96%逐渐升高为接近100%的水平。随后的70次循环中, 容量开始缓慢下降, 直到第140圈, 全电池的容量保持率为92%, 且库伦效率一直维持接近100%的水平。尽管全电池的截止充电电压高达2 V, 远远超过了水的理论分解电压(1.23 V), 但还能维持高库伦效率, 显示了Na-H2O-PEG电解液在水系钠离子电池中的优势。
表3 不同水系钠离子全电池的能量密度对比
Table 3
| Cathode | Anode | Energy density/ (Wh·kg-1) | Ref. |
|---|---|---|---|
| Na0.44MnO2 | NaTi2(PO4)3 | 33 | [39] |
| Na2Ni[Fe(CN)6] | NaTi2(PO4)3 | 43 | [13] |
| Na2Cu[Fe(CN)6] | NaTi2(PO4)3 | 48 | [40] |
| NaMnO2 | NaTi2(PO4)3 | 30 | [12] |
| K0.27MnO2 | NaTi2(PO4)3 | 55 | [41] |
| NaFePO4 | NaTi2(PO4)3 | 61 | [42] |
| Na2VTi(PO4)3 | NaTi2(PO4)3 | 68 | [43] |
| Na3MnTi(PO4)3 | NaTi2(PO4)3 | 82 | [44] |
| Na0.66Mn0.66Ti0.34O2 | NaTi2(PO4)3 | 76 | [45] |
| Na2Ni0.4Co0.6[Fe(CN)6] | NaTi2(PO4)3 | 121 | [46] |
| Fe4[Fe(CN)6]3 | NaTi2(PO4)3 | 126 | This work |
3 结论
本研究通过简单便捷的水热法, 成功合成出高质量、低缺陷的Fe4[Fe(CN)6]3纳米材料。XRD测试结果表明材料为面心立方(fcc)结构, 属于Fm-3m空间点群。SEM和TEM测试结果表明, 所合成出的Fe4[Fe(CN)6]3结晶性优异, 材料呈典型的立方体结构, 边长约500 nm, 材料表面光滑均匀且无严重堆积现象。相比用传统方法合成的低质量Fe4[Fe(CN)6]3, 本文合成的Fe4[Fe(CN)6]3有效减少了空位缺陷并且调节了材料中的结晶水, 从而使得材料具有优异的电化学性能:1C倍率下的比容量高达124 mAh·g-1, 2C、5C、10C、20C、30C和40C倍率下的比容量分别为124、118、105、94、83、74和64 mAh·g-1, 表现出优异的倍率性能; 以5C倍率循环500次, 容量保持率接近100%, 表现出极佳的循环稳定性。以Fe4[Fe(CN)6]3和磷酸钛钠分别为正负极的全电池的工作电压高达1.9 V, 能量密度可达到126 Wh·kg-1。在5C倍率下恒流充放电140次后全电池容量保持率为92%, 且库伦效率接近100%。以这种环保、便捷的方法合成的Fe4[Fe(CN)6]3有望用作水系钠离子电池的正极材料。
参考文献
Water-mediated cation intercalation of open-framework indium hexacyanoferrate with high voltage and fast kinetics
Towards high-voltage aqueous metal-ion batteries beyond 1.5 V: the zinc/zinc hexacyanoferrate system
Thermodynamic analysis on energy densities of batteries
A new class of solvent-in-salt electrolyte for high-energy rechargeable metallic lithium batteries
"Water-in-salt" electrolyte enables high-voltage aqueous lithium-ion chemistries
Rechargeable hybrid aqueous batteries
Recent progress in aqueous lithium- ion batteries
Raising the cycling stability of aqueous lithium-ion batteries by eliminating oxygen in the electrolyte
Aqueous lithium-ion battery LiTi2(PO4)3/LiMn2O4 with high power and energy densities as well as superior cycling stability
Hybrid aqueous energy storage cells using activated carbon and lithium-ion intercalated compounds III capacity fading mechanism of LiCo1/3Ni1/3Mn1/3O2 at different pH electrolyte solutions
An aqueous sodium ion hybrid battery incorporating an organic compound and a prussian blue derivative
An aqueous rechargeable sodium ion battery based on a NaMnO2-NaTi2(PO4)3 hybrid system for stationary energy storage
A low-cost and environmentally benign aqueous rechargeable sodium-ion battery based on NaTi2(PO4)3-Na2NiFe(CN)6 intercalation chemistry
Investigation of the mechanism of Mg insertion in birnessite in nonaqueous and aqueous rechargeable Mg-ion batteries
Highly reversible zinc-ion intercalation into chevrel phase Mo6S8 nanocubes and applications for advanced zinc-ion batteries
An aqueous zinc-ion battery based on copper hexacyanoferrate
Energetic zinc ion chemistry: the rechargeable zinc ion battery
An aqueous rechargeable Zn//Co3O4 battery with high energy density and good cycling behavior
A prussian blue/zinc secondary battery with a bio-ionic liquid-water mixture as electrolyte
High-voltage Zn/LiMn0.8Fe0.2PO4 aqueous rechargeable battery by virtue of "water- in-salt" electrolyte
A rechargeable Na-Zn hybrid aqueous battery fabricated with nickel hexacyanoferrate and nanostructured zinc
Ultrafast alkaline Ni/Zn battery based on Ni-foam-supported Ni3S2 nanosheets
A NaV3(PO4)3@C hierarchical nanofiber in high alignment: exploring a novel high-performance anode for aqueous rechargeable sodium batteries
Vacancy-free prussian blue nanocrystals with high capacity and superior cyclability for aqueous sodium-ion batteries
Surfactant-free aqueous synthesis of pure single-crystalline SnSe nanosheet clusters as anode for high energy-and power-density sodium-ion batteries
Ion-selective copper hexacyanoferrate with an open-framework structure enables high-voltage aqueous mixed-ion batteries
Prussian blue: a new framework of electrode materials for sodium batteries
Sodium iron hexacyanoferrate with high Na content as a Na-rich cathode material for Na-ion batteries
Copper hexacyanoferrate battery electrodes with long cycle life and high power
A superior low-cost cathode for a Na-ion battery
High-quality prussian blue crystals as superior cathode materials for room-temperature sodium-ion batteries
Mesoporous prussian blue analogues: template-free synthesis and sodium-ion battery applications
Nickel hexacyanoferrate nanoparticle electrodes for aqueous sodium and potassium ion batteries
Formation of Fe2O3 microboxes with hierarchical shell structures from metal-organic frameworks and their lithium storage properties
Low-defect prussian blue nanocubes as high capacity and long life cathodes for aqueous Na-ion batteries
Highly crystallized Na2CoFe(CN)6 with suppressed lattice defects as superior cathode material for sodium-ion batteries
Prussian green: a high rate capacity cathode for potassium ion batteries
Prussian blue without coordinated water as a superior cathode for sodium-ion batteries
Towards high power high energy aqueous sodium-ion batteries: the NaTi2(PO4)3/Na0.44MnO2 system
Energetic aqueous rechargeable sodium-ion battery based on Na2CuFe(CN)6-NaTi2(PO4)3 intercalation chemistry
High-performance aqueous sodium-ion batteries with K0.27MnO2 cathode and their sodium storage mechanism
Electrochemical characterization of NaFePO4 as positive electrode in aqueous sodium-ion batteries
High-performance aqueous symmetric sodium-ion battery using NASICON-structured Na2VTi(PO4)3
An aqueous symmetric sodium- ion battery with NASICON-structured Na3MnTi(PO4)3
A novel high capacity positive electrode material with tunnel-type structure for aqueous sodium- ion batteries
Electrochemical properties and redox mechanism of Na2Ni0.4Co0.6Fe(CN)6 nanocrystallites as high-capacity cathode for aqueous sodium-ion batteries