作者简介: 马向荣(1981-), 男, 硕士研究生, 讲师. E-mail:maxiangrong615@163.com
Co2+/Ni2+/Fe3+摩尔比为0.5/3/1, 采用络合剂柠檬酸三钠协助均相沉淀技术, 制备了Co2+-Ni2+-Fe3+-LDHs层状材料, 研究了柠檬酸三钠用量对Co2+-Ni2+-Fe3+ LDHs层间距及形貌的影响。在此基础上, 研究了不同层间距和不同形貌Co2+-Ni2+-Fe3+- -LDHs层状材料的离子交换性能, 即Co2+-Ni2+-Fe3+-
-LDHs层状材料的离子交换性能, 即Co2+-Ni2+-Fe3+-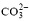 LDHs层状材料在NaCl-HCl的离子交换体系中进行阴离子交换反应, 生成Co2+-Ni2+-Fe3+-Cl--LDHs层状材料。研究结果表明: 当柠檬酸三钠用量为0.6~1.0 mmol/L时, 所制备的LDHs层间距为0.776 nm, 片层结构分散性较好, 产物的较大层间距和较好形貌使其仍保持良好的离子交换性能, 并通过离子交换反应可分别得到
LDHs层状材料在NaCl-HCl的离子交换体系中进行阴离子交换反应, 生成Co2+-Ni2+-Fe3+-Cl--LDHs层状材料。研究结果表明: 当柠檬酸三钠用量为0.6~1.0 mmol/L时, 所制备的LDHs层间距为0.776 nm, 片层结构分散性较好, 产物的较大层间距和较好形貌使其仍保持良好的离子交换性能, 并通过离子交换反应可分别得到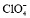 、
、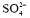 、
、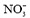 、
、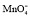 及CH3(CH2)11
及CH3(CH2)11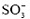 插层Co2+-Ni2+-Fe3+-LDHs层状衍生材料; 当柠檬酸三钠用量在1.5 mmol/L时, 所制备的LDHs层间距为0.770 nm和0.691 nm, 片层结构团聚并成玫瑰花形貌, 使得客体离子较难插入到层间, 产物的离子交换性能降低; 当柠檬酸三钠的量增加到3.0 mmol/L时, 得到的LDHs层间距为0.681 nm, 片层结构变小, 团聚现象加剧, LDHs片完全交错生长成球状形貌, 产物完全失去了离子交换性能。
插层Co2+-Ni2+-Fe3+-LDHs层状衍生材料; 当柠檬酸三钠用量在1.5 mmol/L时, 所制备的LDHs层间距为0.770 nm和0.691 nm, 片层结构团聚并成玫瑰花形貌, 使得客体离子较难插入到层间, 产物的离子交换性能降低; 当柠檬酸三钠的量增加到3.0 mmol/L时, 得到的LDHs层间距为0.681 nm, 片层结构变小, 团聚现象加剧, LDHs片完全交错生长成球状形貌, 产物完全失去了离子交换性能。
Co2+-Ni2+-Fe3+- -LDHs (layered double hydroxides, LDHs) materials were synthesized by using trisodium citrate (TSC) assisted homogeneous precipitation technology. The influences of TSC amount on the basal spacing and morphology of the obtained materials were investigated by changing TSC amount from 0.6 mmol/L to 3.0 mmol/L. Then the deintercalation of carbonate ions from a Co2+-Ni2+-Fe3+-
-LDHs (layered double hydroxides, LDHs) materials were synthesized by using trisodium citrate (TSC) assisted homogeneous precipitation technology. The influences of TSC amount on the basal spacing and morphology of the obtained materials were investigated by changing TSC amount from 0.6 mmol/L to 3.0 mmol/L. Then the deintercalation of carbonate ions from a Co2+-Ni2+-Fe3+--LDHs materials with different basal spacing and shape morphology were investigated by socking in a NaCl-HCl mixed solution. The results indicated that LDHs with basal spacing of 0.776 nm and well-defined hexagonal shapes was obtained when TSC optimized amount was between 0.6-1.0 mmol/L, exhibiting a good anion exchange property. Thus a series of materials intercalated by
,
,
,
and CH3(CH2)11
anions were obtained. When TSC amount was up to 1.5 mmol/L, a new layered structure of LDHs with basal spacings of 0.770 nm and 0.691 nm was observed with rose-like morphology consisting of reunion hexagonal shapes, decreasing its anion exchange property. When TSC amount was further increased to 3.0 mmol/L, the layered structure of LDHs with a basal spacing of 0.681 nm was observed with ball-shaped like morphology consisting of reunion hexagonal shapes, leading to its anion exchange property disappear.
水滑石又称为双羟基复合金属氧化物(Layered double hydroxides, 简称 LDHs), 是一种典型的无机层状化合物。它是由层状主体和层间客体复合而成, 层与层之间一般通过静电引力结合在一起[1], 这种独特的结构和性质受到学术界的广泛关注。LDHs 具有层间阴离子的可交换性[2], 各种无机、有机、杂多酸阴离子、配合物阴离子等均可插入到 LDHs层间, 从而获得各种不同结构的功能新材料[3]。这些复合材料广泛应用于催化、催化剂载体[4, 5, 6]、化工分离、吸附、离子交换、光化学、电磁化学等领域[7, 8, 9, 10]。因此, LDHs层状化合物的制备及其离子交换反应研究已成为无机功能材料领域研究的热点之一[11]。
最近几年, 随着LDHs制备技术的发展, LDHs的种类急剧增加, 特别是过渡金属元素尤其是含铁系元素LDHs以其独特的光、电、磁、催化等性质[12], 成为研究的重点, 并开发了一系列含铁、钴、镍元素LDHs的合成方法。均相沉淀技术是制备LDHs最有效的方法之一, 它是在共沉淀法基础上发展起来的, 即用金属盐作为原料, 尿素作为沉淀剂制备高结晶度形貌规整的层状材料[13]。到目前为止, 采用该方法已合成了一系列Fe2+-Al3+LDHs、Ni2+-Al3+ LDHs、Co2+-Al3+ LDHs、Ni2+-Co2+-Al3+ LDHs、Zn2+-Co2+-Al3+ LDHs等层状材料[14]。由于均相沉淀法主要利用Al3+的两性, 所以该方法主要局限于M2+-Al3+ LDHs 铝系层状材料的制备, 而用均相沉淀法制备M2+-Fe3+ LDHs铁系层状材料一直是研究者追求的目标。但是Fe3+不具有两性特征, 且Fe(OH)3酸性弱于Al(OH)3, 在碱性条件下较难溶解, 不利于LDHs的形成。另外, 由于Fe3+沉淀的pH比二价金属离子低, 决定了Fe3+和二价金属离子并不能同时沉淀形成高结晶度、规则形貌的LDHs[15]。为了提高Fe3+沉淀的pH, 在反应体系中加入络合剂柠檬酸三钠(TSC)来协助Fe3+沉淀, 可以制备结晶度高、形貌规则的铁系LDHs层状材料。但是该铁系LDHs层状材料层间阴离子主要是 

本工作以柠檬酸三钠为络合剂, 采用络合剂协助均相沉淀技术制备了含铁系元素的Co2+- Ni2+- Fe3+- 




1.1.1 试剂
实验所用CoCl2· 6H2O、 NiCl2· 6H2O、 FeCl3· 6H2O、尿素、NaCl、HCl、柠檬酸三钠(C6H5Na3O7· H2O)、NaClO4、Na2SO4、NaNO3、NaMnO4和CH3(CH2)11SO3Na均为分析纯试剂。合成过程及洗涤用水均为去离子水(电导率小于1× 10-6 S/ cm)。
1.1.2 分析表征
采用Rigaku D/Max 2550 VB +/PC型粉末衍射仪对样品进行XRD物相分析, 测试条件: Cu Kα 靶(λ =0.15406 nm), Ni 滤波, 电压 40 kV, 电流 40 mA, 扫描范围2° ~70° (2θ ), 扫描速度5° /min。采用德国 Bru-c--her公司 EQUI NX55 型红外光谱仪, 400~4000 cm-1, 溴化钾压片法测定试样的红外光谱。采用荷兰Philips-FEI公司Quanta 200环境扫描电镜观察样品形貌。采用日本岛津公司AA-6800型原子吸收分光光度计进行镍、钴和铁含量的测定。试样中的C元素含量通过德国元素分析系统公司Vario EL III型元素分析仪进行分析, Cl元素含量通过德国Vario Micro微量元素分析仪进行分析。
1.2.1 不同Co2+-Ni2+-Fe3+-CO32-LDHs层状材料的制备
以Co2+、Ni2+、Fe3+、Co(NH2)2摩尔比为0.5:3.0:1:10, 分别称取四份0.1184 g CoCl2· 6H2O、0.7132 g NiCl2· 6H2O、0.2704 g FeCl3· 6H2O和0.6006 g CO(NH2)2溶解在100 mL去氧超纯水中, 向配制的混合溶液中分别加入0.0168、0.0280、0.0392和0.0840 g的柠檬酸三钠固体, 使反应体系柠檬酸三钠浓度分别为0.6、1.0、1.5、3.0 mmol/L。搅拌均匀后转移到聚四氟乙烯高压反应ss釜中, 通入氮气排尽反应釜中的空气后密封, 150℃水热处理两天, 得到的沉淀经洗涤、过滤、室温干燥后产品分别记为S1-LDHs、S2-LDHs、S3-LDHs、S4-LDHs。
1.2.2 不同Co2+-Ni2+-Fe3+- 

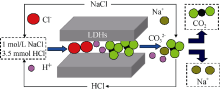
配置500 mL浓度为1 mol/L NaCl和3.5 mmol/L HCl的混合溶液, 将所配制的NaCl-HCl混合溶液加入到500 mL烧瓶中。取0.5 g S1-LDHs产品加入到此混合溶液中, 通氮气排出烧瓶中的空气后将烧瓶密封, 磁力搅拌一天。离子交换后的产物在有氮气保护条件下经洗涤、过滤和干燥得到Co2+-Ni2+- Fe3+-Cl-LDHs层状材料, 该产品记为D1-LDHs。采用同样的方法对产物S2-LDHs、S3-LDHs、S4-LDHs进行 

1.2.3 不同阴离子插层Co2+-Ni2+-Fe3+LDHs层状材料的制备
配置500 mL浓度为2.5 mol/L的NaClO4溶液, 称取0.5 g已成功脱除 
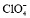
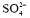
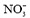
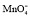
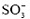
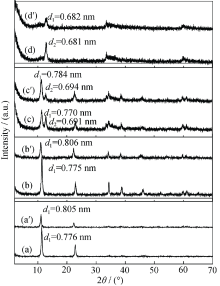
图1为不同柠檬酸三钠用量所得产物的XRD图谱, 从图中可以看出, 所得试样均显示出LDHs的特征衍射峰, 没有发现其他杂相衍射峰, 表明制备得到了纯相三元组分Co2+-Ni2+-Fe3+- 




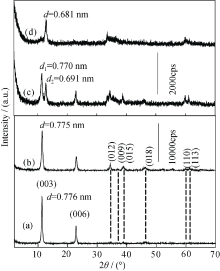 | 图 1 不同TSC用量制备的LDHs产物的XRD 图谱Fig. 1 XRD patterns of the products prepared with various TSC amounts(a) S1-LDHs; (b) S2-LDHs; (c) S3-LDHs; (d) S4-LDHs |
通过对产物S1-LDHs、S2-LDHs、S3-LDHs、 S4-LDHs的Co2+、Ni2+、Fe3+金属元素进行分析检测, 发现Co2+/Ni2+/Fe3+摩尔比从1.00/6.00/2.00逐渐变为1.00/5.04/2.03(表1), Ni2+相对含量减少, Fe3+的相对含量增加, 这主要是由于反应体系中存在过量的柠檬酸三钠时, 它除了与Fe3+络合外, 还与Ni2+络合并生成络合物。Ni(OH)2溶度积常数大于Fe (OH)3, 在较高pH条件下, 过量的柠檬酸三钠使部分Ni2+仍以络合物形式存在, 导致了Ni2+的流失, LDHs的层板结构中Fe3+的相对含量增加, 正电荷也随之增加, 它对阴离子的引力也增大, 从而使LDHs层间距(d003间距)从0.776 nm降低为0.681 nm。
| 表 1 不同TSC浓度下所得产物Co/Ni/ Fe的摩尔比及用HCl-NaCl处理后的产物 C、Cl元素含量分析结果 Table 1 Co2+/Ni2+/ Fe3 molar ratios in samples prepared with different TSC amounts and analysis on C and Cl elements in samples treated with a NaCl-HCl mixed solution |
2.2 不同Co2+-Ni2+-Fe3+- 

在相同条件下, 不同层间距LDHs的离子交换性能也不同, 为此选用层间距不同的S1-LDHs、S2-LDHs、S3-LDHs、S4-LDHs, 对其进行离子交换研究, 脱除过程示意图如图2所示: 将产物在NaCl-HCl混合溶液中进行处理, 层间 





图3为S1-LDHs、S2-LDHs、S3-LDHs、S4-LDHs在NaCl-HCl混合溶液处理后产物的XRD图谱。S1-LDHs、S2-LDHs经溶液处理后得到的D1-LDHs、D2-LDHs, 其(003)衍射峰向低角度偏移, 表明处理后的产物层间距发生了变化, 分别从0.776、0.775 nm增大到0.805、0.806 nm(图3(a° )、3(b° ))。D1-LDHs、D2-LDHs的元素含量分析表明其C元素含量很低, 仅为0.001%和0.002%, 而Cl元素含量分别增加到6.841%和6.953%, 说明体积较小的 


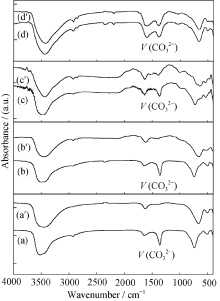
D1-LDHs、D2-LDHs、D3-LDHs、D4-LDHs的FT-IR图谱如图4所示, 从图中可以看出: D1-LDHs、D2-LDHs在1360 cm− 1处没有观察到 




图5为不同柠檬酸三钠用量所得产物的SEM照片, 从图中可以看出, 随着柠檬酸三钠的浓度逐渐增加, 所得产物的形貌发生明显变化。当柠檬酸三钠浓度为0.6 mmol/L时, 产物(S1-LDHs)的形貌呈平面尺寸300 nm且均匀分散的六边形片层结构(图5(a)), 此时由于产物的分散性好, 层间通道极易被体积大的离子撑大, 所以客体Cl-能容易地插入到LDHs层间。图(3(a)、(a¢ ))和图(4(a)、(a¢ ))证明该产物层间 


 | 图 5 不同TSC用量制备的LDHs产物的SEM照片Fig. 5 SEM images of the products prepared at various TSC amounts(a) S1-LDHs; (b) S2-LDHs; (c) S3-LDHs; (d) S4-LDHs |
综上所述, 通过对产品S1-LDHs、S2-LDHs、S3-LDHs、S4-LDHs及其在离子交换过程中的产物D1-LDHs、D2-LDHs、D3-LDHs、D4-LDHs进行分析, 发现柠檬酸三钠的用量影响所制备材料的晶相、层间距及形貌, 进而影响其离子交换性能和层间 
利用LDHs独特的阴离子可交换性, 可以制备不同阴离子插层LDHs的衍生材料。S1-LDHs、S2-LDHs层状材料经NaCl-HCl溶液处理后完全实现了 

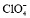
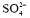
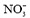
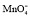
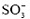
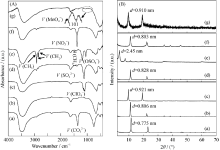 | 图 6 不同阴离子插层的产物Co2+-Ni2+-Fe3+-LDHs的FT-IR图谱(A)和XRD图谱(B)Fig. 6 FT-IR spectra (A) and XRD patterns (B) of Co2+- Ni2+-Fe3+-LDHs incorporated by different anions |
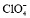
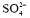
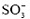
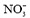
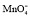
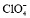
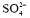
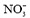
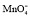

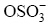
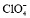
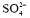
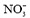
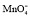
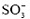

1) 柠檬酸三钠用量控制在0.6~1.0 mmol/L时, LDHs层板结构中Ni2+、Co2+、Fe3+含量接近投料比, 层间距(d003间距)较大(0.776 nm), 且为均匀分散的六边形片层结构, 使其具有了良好的离子交换性能, 通过离子交换反应可得到不同阴离子插层的层状衍生材料。
2) 提高柠檬酸三钠的用量时, 过量的柠檬酸三钠与Ni2+络合, 导致了Ni2+的流失, 使得LDHs的层板结构中Fe3+的相对含量增加, 正电荷密度增加, 对阴离子的引力也增大, 层间距降低(0.698 nm), 离子交换性能下降。此外, 伴随着层间距降低的同时, 产物片层结构出现团聚现象。如果LDHs片层结构通过“ 共边” 形式全部生长在一起, 层间通道不能随着阴离子的插入而增大, 会使其完全失去离子交换性能。
3) 采用柠檬酸三钠成功制备和控制Co2+-Ni2+- Fe3+-LDHs的层间距、形貌等微观结构, 极大地拓展和延伸了LDHs的应用领域, 为其他含铁类LDHs的研究奠定了理论基础。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|