翟倩倩(1988-), 女, 硕士研究生. E-mail:jimoxinqing_28@126.com
为了探究仿生纳米含硅羟基磷灰石的合成条件及含硅量对其结晶性能的影响, 以Ca(NO3)2、(NH4)2HPO4和Si(OCH2CH3)4(TEOS)为原料, 采用化学沉淀法制备了不同含硅量的羟基磷灰石, 并通过傅里叶变换红外光谱(FTIR)、X射线荧光光谱(XRF)、X射线衍射(XRD)、透射电镜(TEM)对材料进行了表征。结果表明较低温(40℃)时有利于合成纯净的仿生纳米含硅羟基磷灰石, SiO44-取代部分PO43-进入羟基磷灰石的晶格。随着含硅量的增加, 仿生纳米含硅羟基磷灰石的结晶度和晶粒尺寸均降低, 晶胞参数
To explore the synthesis condition of the bionic nano-silicon-substituted hydroxyapatite and the impact of the silicon content on its crystallization properties, hydroxyapatite of different silicon content were synthesized from Ca(NO3)2, (NH4)2HPO4 and Si(OCH2CH3)4(TEOS)
羟基磷灰石(Ca10(PO4)6(OH)2, Hydroxyapatite, HA)是脊椎动物骨和牙齿中的主要无机成分[ 1], 比如人体骨中HA的重量大约占60%, 人牙齿的珐琅质表面HA的重量占95%以上。人工合成的HA植入人体后, 在体液的作用下, 钙和磷游离出材料表面, 并与人体骨组织形成化学键合, 参与新组织的形成, 因此HA具有良好的生物相容性。
然而相对于其他生物材料, 人工合成的HA的缺点是它与骨骼之间的反应活性和整合速率相对较低, 这意味着病人需要更长的康复时间[ 2], 而掺杂硅的HA表面成骨细胞的增殖速度比纯HA快[ 3]。实际上, 人体内的天然HA并不是纯HA, 而是含有CO32-和钠、镁、硅、锶、锌等离子, 因此需要向作为骨修复材料的HA中仿生添加其他的元素, 含硅HA(Ca10(PO4)6- x(SiO4) x(OH)2- x,Si-HA)就是其中一种仿生HA。
Si-HA和HA具有相同的结构, 只是Si-HA部分PO43-被SiO44-取代。目前已有几种方法合成Si-HA, 如溶胶-凝胶法[ 4]、水热合成法[ 5]、固相反应法[ 6]、湿法[ 7, 8]、控制结晶法[ 9]等。Tian等[ 7]采用湿法成功合成了Si-HA, 硅的掺入引起了晶胞参数的变化, 并通过模拟体液法证实了Si-HA具有良好的生物活性。Bianco等[ 8]同样采用湿法合成了针状的Si-HA, 高温煅烧下表现出了良好的热稳定性。Balas等[ 9]采用控制结晶法合成了Si-HA, 并通过标准模拟体液法证明了Si-HA比普通HA具有更好的生物相容性。但是前人大多对合成的Si-HA进行高温煅烧, 高温煅烧会使结晶度提高, 晶粒尺寸变大, 而自然骨中HA的基本特点是缺钙、低结晶度、小尺寸、晶格中含CO32-[ 10], 因此高温煅烧背离了Si-HA作为骨替代材料的初衷。Niwa[ 11]指出随着煅烧温度的升高, HA沉积骨的能力降低, 因此从仿生和提高生物活性的角度出发, 在制备HA的过程中应避免高温煅烧。因此, 本研究以Ca(NO3)2、(NH4)2HPO4和Si(OCH2CH3)4(TEOS)为主要原料, 研究讨论了未煅烧Si-HA的合成及含硅量对其化学组成、晶相等的影响。
Si-HA中的SiO44-取代PO43-, 部分OH-流失以维持电荷平衡, 生成了Ca10(PO4)6- x(SiO4) x(OH)2- x。其反应机理可用下式表示:(NH4)2HPO4+NH4OH=(NH4)3PO4+H2O
3(NH4)3PO4+NH4OH=(NH4)10(PO4)3OH
2(NH4)10(PO4)3OH+10Ca(NO3)2=Ca10(PO4)6(OH)2+
20NH4NO3
Ca10(PO4)6(OH)2+ xSiO44-=Ca10(PO4)6- x(SiO4) x(OH)2- x+ xPO43-+ xOH-
实验分为三个部分, 第一部分: 研究能否根据上述原理合成Si-HA, 并探讨实验温度对Si-HA结晶性能的影响, 陈化24 h, 分别在40℃、50℃、60℃反应温度下合成含硅12%的Si-HA; 第二部分: 研究陈化时间对Si-HA结晶性能的影响, 固定反应温度为60℃, 分别在陈化时间为24、48、72 h条件下合成含硅12%的Si-HA; 第三部分: 研究含硅量对Si-HA结晶性能的影响, 在40℃反应温度, 24 h陈化时间条件下变换含硅量分别为0、2%、7%、12%、17%, 所得产物分别记为HA、2%Si-HA、7%Si-HA、12%Si-HA、17%Si-HA, 样品含硅量以 n(Si)/( n(Si)+ n(P))计算。
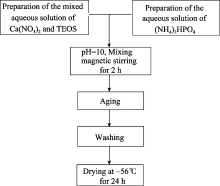
以Ca(NO3)2、(NH4)2HPO4和TEOS为主要原料,用氨水调节pH=10。各试剂的用量以硅能取代HA中的磷为前提计算, 保持 n(Ca)/( n(Si) + n(P))=1.67。各反应物的用量见表1。先将Ca(NO3)2和(NH4)2HPO4配成相同浓度的水溶液, 将计算量的TEOS加入Ca(NO3)2水溶液中, 搅拌均匀。一定温度下, 将(NH4)2HPO4水溶液滴入Ca(NO3)2水溶液中, 同时用氨水维持pH=10。继续搅拌2 h, 然后在相应温度下陈化一定时间, 水洗除去水溶性杂质, -56℃下冷冻干燥24 h得到白色粉末状产物。实验流程如图1所示。
| 表1 试剂用量 Table 1 Quantities of used reactants |
FTIR采用德国Bruker公司生产的VECTOR 22 FTIR红外光谱仪测试样品的振动光谱, 分辨率为4 cm-1在4000~400 cm-1波长范围内进行扫描, 取32次平均值; 元素分析采用德国布鲁克AXS公司生产的S8 TIGER型X射线荧光光谱仪(XRF)测定; XRD采用日本Rigaku D/max-c型X射线衍射仪测试样品的物相、晶型, Ni滤波, Cu Kα辐射源, X射线波长λ=0.1541 nm, 加速电压和电流强度分别为40 kV和70 mA, 设定扫描间隔为0.02°, 扫描速度为4°/min; TEM采用JEM-1011型低分辨透射电子显微镜, 点分辨率: 0.3 nm, 线分辨率: 0.14 nm, 加速电压为100 kV。
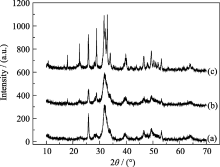
不同反应温度下12%Si-HA的XRD图谱如图2, 比较(a)、(b)、(c)三图谱可以看出a、b两图谱非常相似, (211)(112)(300)晶面的衍射峰没有分开, 说明Si-HA的结晶度较低; 峰形不尖锐且明显宽化, 说明晶粒尺寸较小; 但前者的(002)晶面衍射峰比后者更尖锐, 说明前者 c轴晶粒尺寸更大, 从而晶粒长径比更大。天然HA呈针状或棒状, 因此, 40℃的Si-HA与自然HA更相似。(c)图峰形比较尖锐, 因而晶粒尺寸较大; (211)(112)(300)晶面的衍射峰部分分开, 因而结晶度较高, 同时含有杂质峰, 说明高温不适合合成纯净的Si-HA。综上所述, 且从仿生的角度出发, 选择接近人体温度的40℃作为合成仿生Si-HA的最佳温度。
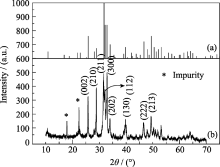
单独分析60℃、陈化24 h的12%Si-HA如图3(b)所示。图3(a)的竖线代表PDF标准卡片中HA的标准谱线。以(002)、(210)、(211)、(112)、(300)为代表的衍射峰相对于标准峰向小角方向偏移。这是因为SiO44-取代PO43-进入晶格, Si-O键长(0.161 nm)比P-O键长(0.155 nm)长, 造成晶格间距 d扩大, 根据Brag公式 λ=2 dsin θ, 当X射线波长 λ一定时, 衍射角 θ向小角度偏移。左侧2 θ=17.9º和2 θ=22.4º处有两个杂质峰。
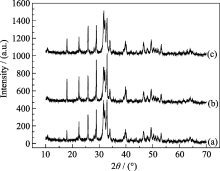
如图4, (a)、(b)、(c)三图谱在峰位置、峰强度等方面均比较相似, 说明陈化时间对Si-HA的结晶性能基本没有影响。
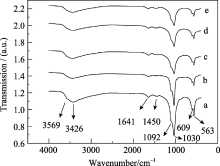
图5是HA、2%Si-HA、7%Si-HA、12%Si-HA、17%Si-HA的红外图谱。3569 cm-1是羟基吸收峰, 3426 cm-1处的宽峰是水的吸收峰, 1641、1450 cm-1为碳酸根的ν3振动吸收峰, 1092、1030 cm-1是磷酸根的ν3振动吸收峰, 609、563 cm-1为磷酸根的ν4振动吸收峰。随着TEOS含量的增加, OH-和PO43-的吸收峰呈减弱趋势, 以致于含硅量较高时OH-峰几乎完全被3426 cm-1处的宽峰覆盖。由于硅的离子半径和磷的离子半径接近, 故可以部分取代HA晶格中的磷, 因而SiO44-部分取代PO43-进入HA的晶格中, 同时部分OH-流失以维持电荷平衡。CO32-的存在是因为碱性溶液在反应过程中吸收了空气中的CO2。
XRF测得硅和钙元素的含量如表2所示, 硅含量比理论含量偏低, 说明硅没有完全进入Si-HA晶格, 部分硅残留在了溶液中。钙也比理论值低, 说明产物是与自然HA相似的缺钙Si-HA。
| 表2 Si-HA的Ca和Si元素含量 Table 2 The content of Ca and Si of Si-HA |
HA、2%Si-HA、7%Si-HA、12%Si-HA、17%Si-HA的XRD图谱的对比如图6所示, 底部的竖线是PDF标准卡片中HA的标准谱线, 可以看出测得的Si-HA衍射峰与PDF标准谱线基本吻合, 说明得到了较为纯净的目标产物。但是在2 θ为31.773º、32.196º、32.902º的(211)、(112)、(300)晶面的衍射峰没有完全分开, 说明HA的结晶度较低, 且衍射峰明显宽化, 说明晶粒尺寸较小, 这与骨和牙本质中的天然HA的XRD峰基本吻合[ 10]。五种HA的图谱很相似, 随着含硅量的增加, 峰形的尖锐程度降低, 峰宽增加, 说明随着含硅量的增加HA的结晶度降低、晶粒尺寸减小, 与天然HA更相似。
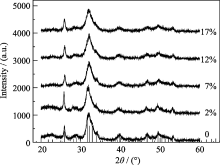 | 图6 不同含硅量的Si-HA的XRD衍射图谱Fig. 6 XRD patterns of (a) HA, (b) 2%Si-HA, (c) 7%Si-HA, (d) 12%Si-HA and (e) 17%Si-HA |
根据Scherrer公式和(002)晶面衍射峰(2 θ=25.8º)的半高宽计算 c轴晶粒尺寸, 用Jade软件求平均晶粒尺寸, 如表3所示, 2%Si-HA的 c轴晶粒尺寸最大, 但整体上随着硅含量的增加呈减小趋势。平均晶粒尺寸也随硅含量的增加而减小。这可能是由于Si-O键长(0.161 nm)比P-O键长(0.155 nm)长, 所以少量的SiO44-取代PO43-可能会引起晶粒尺寸稍微增大, 随着取代量的增加, 引入结晶缺陷, 抑制晶体增长, 晶粒尺寸减小。
| 表3 Si-HA的 c轴及平均晶粒大小 Table 3 Grain size of c-axis and average grain size of Si-HA |
用Jade软件对XRD图谱进行全谱拟合、精修得到晶胞参数值如表4所示, 随着含硅量的增加, 晶胞参数 a、 c均增大, 与Balas[ 9]的研究结果一样, 其中2%Si-HA的 c值增加幅度较大。SiO44-四面体体积比PO43-四面体大, SiO44-的引入造成晶胞参数增大。
| 表4 HA、Si-HA的晶胞参数 Table 4 Lattice parameters of HA and Si-HA |
将Si-HA在水中的悬浮液超声分散, 用铜网捞取适量, 置于透射电镜下观察, 如图7所示, Si-HA分散性较好, 大小均匀, 长度约为20~80 nm, 宽度约为10 nm, 呈针状或棒状, 衬度较小, 结晶度较低。
以Ca(NO3)2、(NH4)2HPO4和TEOS为原料, 采用化学沉淀法合成了Si-HA。表征结果表明较低温(40℃)有利于合成纯净的Si-HA; 陈化时间对产物的晶体结构基本没有影响; SiO44-取代部分PO43-进入HA的晶格, 含硅量的增加造成结晶度和晶粒尺寸降低、晶胞参数 a和 c增大。总之, 合成的Si-HA为缺钙纳米级颗粒, 且尺寸均匀, 结晶度低, 有少量CO32-, 与天然HA类似。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|