郭 佳(1985-), 女, 硕士, 助理实验员. E-mail:panda3782006@163.com
采用水热法, 无需添加剂, 通过调控反应液pH值和反应温度制备了不同结构和形貌的BiVO4可见光催化剂. 利用X射线衍射(XRD)、扫描电子显微镜(SEM)、紫外-可见漫反射(DRS)和低温氮吸附等手段对样品进行表征, 结果显示: 水热温度与反应液pH值对晶体结构有很大影响, 180℃水热温度和酸性条件有利于单斜相的生成. 反应液pH值对形貌也有很大影响, 不同条件下得到了片状、立方状、棒状等不同形貌的BiVO4. 同时以亚甲基蓝为降解对象, 考察了所制备BiVO4的可见光催化活性. 其中, pH值为2, 反应液中制备的片状单斜相BiVO4具有最高的光催化活性(4 h达92.0%). 此外, 还考察了光催化剂用量、亚甲基蓝浓度和电子受体的存在对光催化过程的影响, 结果表明: 当催化剂用量为1.0 g/L, 亚甲基蓝浓度为10 mg/L, KBrO3为电子受体时光催化效果最佳.
Visible-light photocatalysts BiVO4 with different crystal structures and morphologies were prepared
自1972年Fujishima和Honda报道TiO2光解水后, 光催化技术引起了人们的广泛关注[ 1]. 然而, 大多数报道的半导体光催化剂仅对占太阳能4%的紫外光有响应[ 2], 这大大限制了其应用. 为了解决这一问题, 人们发展了金属或非金属掺杂[ 3, 4]、染料敏化[ 5]等方法来拓展半导体光催化剂的光谱响应范围. 但这些方法又引起了新的问题, 比如: 掺杂半导体催化剂的掺杂中心往往成为光生电子和光生空穴的复合中心, 导致光催化活性的降低[ 6]. 因此目前研究热点转向开发对可见光响应的新型窄带隙半导体催化剂, 如: CaIn2O4[ 7]、Bi2WO6[ 8]、AgAlO2[ 9]、Bi2MoO6[ 10]、InMO4 (M = Nb, Ta)[ 11]等.
钒酸铋(BiVO4)是一种稳定的半导体材料, 禁带宽度相对较窄, 可作为新型可见光响应半导体催化剂用于光解水和光解有机污染物[ 12]. BiVO4有多种制备方法, 如: 固态反应法[ 13]、共沉淀法[ 14]、化学浴沉积法[ 15]、有机金属分解法[ 16]、水热法[ 17]等. 其中, 水热法因其条件温和可控, 引起了人们的关注. 目前有很多报道通过采用水热法并加入表面活性剂或模板剂[ 18, 19, 20]制备出不同形貌和结构的BiVO4, 但表面活性剂或模板剂的加入使其后处理复杂, 给放大生产带来了困难[ 21]. 而无添加剂水热合成不同形貌和结构BiVO4的研究报道还很有限[ 22, 23, 24]. 由于BiVO4的光催化性能与晶体的结构和形貌有关[ 25], 因此研究BiVO4的制备条件与结构、形貌和性能之间的关系具有重要意义, 对于提高BiVO4的可见光催化性能具有重要作用.
本工作采用水热法制备BiVO4, 在制备过程中不加入任何添加剂, 通过控制制备条件得到不同结构和形貌的BiVO4. 以制备的BiVO4为催化剂用于可见光下对亚甲基蓝溶液的光催化降解, 研究制备条件与结构、形貌和性能之间的联系, 同时考察了光催化过程中的各种影响因素.
Bi(NO3)3·5H2O、NH4VO3、HNO3、NaOH、无水乙醇, 均为分析纯, 实验用水为蒸馏水.
样品的物相表征采用MSAL-XRD2型CuKα辐射的X射线衍射仪测定, 电压36 kV, 电流20 mA, 扫描速度为8o/min, 步宽为0.02o, 扫描范围2 θ=10o~ 80o. SEM采用JEOL JSM-6330F扫描电子显微镜测定. 紫外-可见漫反射光谱以BaSO4为空白, 采用Shimadzu UV25紫外-可见漫反射仪测定. 亚甲基蓝溶液的吸收光谱由TU1801型紫外-可见分光光度计测定. 低温氮吸附实验采用Tristar 3000型比表面测定仪测定.
将5.0 mmol (2.45 g) Bi(NO3)3·5H2O溶解在10.0 mL 4.0 mol/L的HNO3溶液中, 同时将5.0 mmol (0.58 g) NH4VO3溶解在10.0 mL 2.0 mol/L的NaOH溶液中, 在剧烈搅拌下将两溶液混合形成黄色澄清溶液, 并使用2.0 mol/L的NaOH调节此溶液的pH值. 搅拌半小时后将前驱体溶液转移至100 mL的聚四氟乙烯不锈钢高压釜中, 并将高压釜放入烘箱中在不同温度下进行水热反应. 反应结束后冷却至室温, 打开水热釜收集所得沉淀, 用蒸馏水和无水乙醇分别洗涤三次, 80℃干燥4 h得到产物.
光催化实验在玻璃夹套式恒温反应器中进行, 降解对象为100 mL亚甲基蓝(MB)溶液. 光源为250 W反射镝灯, 与液面垂直距离为15 cm, 使用400 nm滤光片滤去紫外光. 反应时不断磁力搅拌, 夹层通入冷凝水, 并鼓入空气以提供反应所需氧气. 暗反应0.5 h达到染料与催化剂间的吸附平衡, 此后间隔时间取样, 经高速离心后测定上层清液吸光度.
亚甲基蓝溶液的紫外-可见光谱在 λ= 664 nm处溶液有特征吸收峰, 在一定范围内浓度 C和吸光度 A成正比, 因此可用降解率 D来衡量亚甲基蓝的光致降解率: D=[( A0- A)/ A0]×100%, 式中 A0和 A分别为样品的初始吸光度和降解后的吸光度.
图 1是反应液pH值为4时, 在不同温度下水热2 h后所得BiVO4样品的XRD图谱. 从图1中可以看出未经加热所得的样品为无定形结构. 水热温度为160℃时, 样品具有较好的结晶度, 除了单斜相BiVO4 (m-BiVO4, JCPDS 14-0688)的特征峰, 还在24.37o、32.68o、48.50o伴有四方相BiVO4 (t-BiVO4, JCPDS 14-0133)的特征峰. 当水热温度升高到180℃时, 样品为单一的单斜相BiVO4, 没有其它晶相衍射峰的存在. 这是由于单斜白钨矿结构的热稳定性优于四方锆石结构[ 26], 水热温度越高, 越有利于获得热稳定性高的单斜相.
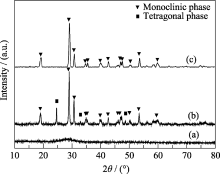 | 图1 不同水热温度下制备BiVO4的XRD图谱Fig. 1 XRD patterns of BiVO4 obtained at different hydrothermal temperatures(a) Room temperature, pH=4; (b) 160℃, pH=4; (c) 180℃, pH=4 |
图2是在180℃不同pH值反应液中水热2 h后所得到产物的XRD图谱, 从图中可以看出, 在酸性条件下(反应液pH值为2、4、6)得到的是单一的单斜相BiVO4, 且均具有较高的结晶度. 在碱性条件下, 当反应液pH值为8时出现了四方相BiVO4特征峰. 当反应体系呈酸性时, 单斜相BiVO4是热稳定相, 但随着反应液pH增大到弱碱性时, 在反应热力学上更倾向于形成四方相BiVO4. 当碱性进一步增加到反应液pH值为10时, 单斜相BiVO4峰明显减弱, 并出现了Bi(OH)3的峰. 这是由于在强碱性条件下, Bi3+倾向于与OH-结合形成更稳定的Bi(OH)3. 通过XRD图谱分析可知, 反应液pH值会影响所制备BiVO4的晶相, 酸性条件有利于高结晶度单斜相BiVO4的形成, 而碱性条件下会有四方相BiVO4甚至是Bi(OH)3的生成.
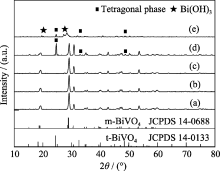 | 图2 不同pH反应液中制备BiVO4的XRD图谱Fig. 2 XRD patterns of BiVO4 obtained in reaction solution with different pH values(a) pH=2, 180℃; (b) pH=4, 180℃; (c) pH=6, 180℃; (d) pH=8, 180℃; (e) pH=10, 180℃ |
为了考察反应液pH值对BiVO4颗粒形貌的影响, 对所得产物进行了电镜表征. 从图 3可以看出, 不同反应液pH值条件下产物的形貌有明显差异. 当反应液pH值为2时, 产物为长约450 nm, 宽约350 nm的片状BiVO4; 当反应液pH为4时, 产物为长约400 nm, 宽约180 nm的片状BiVO4; 当反应液pH值为6时, BiVO4的形貌为规则的立方体, 边长约300 nm; 反应液pH值为8时, BiVO4样品主要为棒状, 长3 μm, 宽约380 nm.
 | 图3 不同pH值反应液中制备BiVO4的SEM照片Fig. 3 SEM images of BiVO4 samples obtained in reaction solution with different pH values(a) pH=2, 180℃; (b) pH=4, 180℃; (c) pH=6, 180℃; (d) pH=8, 180℃ |
由于在反应体系中仅调节了反应液的pH值, 没有添加任何模板剂或表面活性剂, 因此可以推断溶液酸碱性对BiVO4的形貌有重要影响. 改变体系pH值可以控制反应过程中的界面张力(表面自由能), 从而调控纳米晶体生长[ 27]. 根据金属氧化物的酸碱表面性质, 反应液pH值的改变会使沉淀表面的质子浓度发生变化, 进而导致系统界面张力的改变.实验中, 随着反应液pH值的逐渐增大, H+逐渐被中和, BiVO4晶体表面的H+浓度不断改变, 导致在各晶面上的表面自由能差异显著. 具有较高表面自由能的晶面上晶体生长速度较快, 从而引起晶体的各向异性生长, 得到了片状、立方状、棒状等不同形貌的BiVO4.
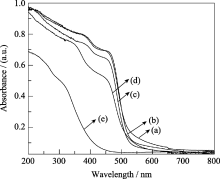
材料对光的吸收范围是影响光催化效果的关键因素之一. 图4是不同反应液pH 条件下制备的BiVO4及四方相BiVO4的紫外-可见漫反射光谱(四方相参照文献[ 28]制备). 反应液pH值为2、4、6时所制备的单斜相BiVO4具有相似的吸收光谱: 在可见光区有陡峭的吸收边缘(分别位于553、526、521 nm); 在475 nm处有一强吸收峰, 在400 nm附近有一弱吸收峰. 四方相BiVO4对光的吸收主要在小于400 nm的紫外光区域, 吸收边带在414 nm. 反应液pH值为8时所制备的BiVO4混晶的吸收光谱是单斜相和四方相光谱的叠加, 吸收边带位于518 nm, 在可见光区域对光的吸收强度比单斜相BiVO4低, 但明显强于四方相BiVO4. 根据吸收边带计算[ 29]出各样品的带隙能分别为2.33 eV (pH=2)、2.36 eV (pH=4)、2.38 eV (pH=6)、2.39 eV (pH=8) 和2.99 eV (t-BiVO4), 与文献报道的带隙能2.4 eV (m-BiVO4)、2.9 eV (t-BiVO4)[ 25]相近.
密度泛函理论对电子结构进行计算表明, 四方相BiVO4对光的吸收带是由电子从O2p轨道(价带)向V3d轨道(导带)跃迁产生的, 而单斜相BiVO4的吸收带是由电子从Bi6s和O2p所形成的杂化轨道(价带)向V3d轨道(导带)跃迁所产生[ 30], 杂化轨道的形成使价带范围变宽, 带隙能变小, 因此单斜相BiVO4的带隙能比四方相BiVO4的带隙能小. 反应液pH值为8时所制备的BiVO4由于是含有单斜相和四方相的混晶, 其带隙能比水热制备的单斜相BiVO4大. 反应液pH值为2、4、6时制备的BiVO4均为单斜相, 因此其表现出相似的吸收光谱.但其带隙能仍有微小差异, 这可能是由于制备时不同的pH条件, 造成了VO43-四面体不同的扭曲程度, 导致各样品的电子结构间存在细微差别[ 24].
2.2.1 BiVO4光催化剂对亚甲基蓝的降解作用
以180℃、pH值为2反应液下水热2 h制备的BiVO4为催化剂, 光降解10 mg/L亚甲基蓝溶液, 催化剂用量为1.0 g/L. 图5显示了降解过程中亚甲基蓝溶液紫外-可见吸收光谱随时间的变化. 在可见光照射下, 亚甲基蓝溶液的紫外吸收光谱强度逐渐降低. 伴随着脱甲基过程, 最大吸收峰从664 nm逐渐移至613 nm, 反应结束后染液颜色基本褪去. 反应1、3和4 h时, 最大吸收峰分别在650、625和613 nm处, 说明亚甲基蓝通过N-脱甲基过程, 分别以天青B、天青A和天青C的形式存在[ 31].
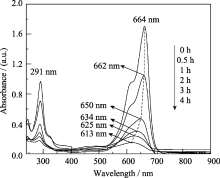 | 图5 亚甲基蓝溶液紫外-可见吸收光谱随时间的变化Fig. 5 Changes of UV-Vis spectra of MB solution with irradiation timeBiVO4 prepared at 180℃ in pH=2 reaction solution for 2 h |
2.2.2 不同反应液pH条件下制备BiVO4的光催化性能比较
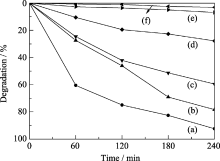
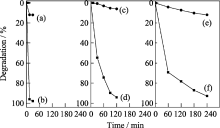
选择浓度为10 mg/L的亚甲基蓝溶液为模拟污染物, 催化剂用量为1.0 g/L, 在可见光下考察不同反应液pH条件下制备BiVO4的光催化活性, 同时进行了光空白和催化剂空白实验, 结果如图6所示. 光空白和催化剂空白实验4 h后, 光催化降解率分别仅为3.1%和6.9%, 说明在亚甲基蓝溶液的降解过程中, 可见光和催化剂二者必须同时存在. 用反应液pH值为2、4、6制备的单斜相BiVO4为催化剂, 光照4 h后, 亚甲基蓝溶液能得到有效降解, 降解率分别为92.0%、78.3% 和59.5%, 而相同条件下, 反应液pH值为8时制备BiVO4的降解率较低, 仅为28.4%.
由于单斜相的光催化活性比四方相的光催化活性高[ 25, 32], 因此, 反应液pH值为2、4、6时得到的单斜相样品的降解率比反应液pH值为8时得到的混合相样品降解率更高.而单斜相样品之间降解率的差异, 一方面可能是比表面积的影响, 反应液pH值为2、4、6时制备的BiVO4比表面积分别为16.0、8.2、3.7 m2/g. 另一方面可能是不同的反应液pH条件下所制备的样品带隙能之间存在差异.
2.2.3 催化剂用量的影响
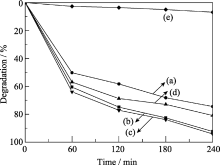
以180℃、pH值为2反应液中水热2 h制备的BiVO4为催化剂, 固定光催化反应其它条件, 考察催化剂用量分别为0.5、1.0、1.5、2.0 g/L时对降解亚甲基蓝溶液效果的影响. 结果如图 7所示: 当BiVO4用量为1.5 g/L时降解率最高, 4 h可达到94.2%. 催化剂用量低于1.5 g/L时, 随着催化剂用量增加, 光催化活性增强. 这是由于随着催化剂用量的增加, 光催化活性中心也增加. 但当催化剂用量为2 g/L时, 降解效果反而有所降低, 4 h降解率仅为80.9%. 这是由于过量的催化剂容易引起光散射, 溶液浊度大, 影响催化剂对光照能量的吸收, 且粉体浓度高时易团聚, 不利于表面活性位点对染料的吸附和对可见光的吸收, 光生电子-空穴数量以及羟基自由基量降低. 另外, BiVO4用量为1.0 g/L时, 其降解效果和用量为1.5 g/L时基本相当. 这是由于尽管光催化活性中心增加, 但此时溶液中催化剂粉体团聚现象严重, 影响了催化剂对光的吸收. 在降解效果相当的情况下, 为避免催化剂的浪费, 以1.0 g/L为最佳催化剂用量.
2.2.4 染料初始浓度的影响
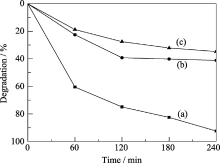
染料初始浓度也是影响光催化降解效率的一个重要因素. 以180℃、pH值为2反应液中水热 2 h制备的BiVO4为催化剂, 固定催化剂投加量为1 g/L, 考察亚甲基蓝溶液的初始浓度分别为10、20、30 mg/L时对光催化降解效果的影响, 结果如图8所示.
随着初始浓度的提高, 亚甲基蓝的降解率呈下降趋势. 10 mg/L亚甲基蓝溶液反应4 h时降解率就可达到92.4%, 而随着初始浓度提高到20和30 mg/L, 反应4 h的降解率仅为 41.1%和34.7%. 这是由于随着初始浓度的提高, 催化剂表面吸附的亚甲基蓝分子数会随之增加, 从而减少了产生羟基自由基的活性点位[ 33], 并且高浓度的染料色度大, 影响溶液的透光率, 阻碍了BiVO4催化剂表面对光的吸收, 导致了亚甲基蓝降解率的降低[ 34]. 实际应用时, 宜选用10 mg/L的亚甲基蓝作为最佳染料初始浓度.
2.2.5 电子受体对光催化效果的影响
光生空穴容易与光生电子复合, 从而导致光催化效果降低. 为保证光催化反应的有效进行, 必须减少光生电子与空穴的简单复合. 由于氧化剂是有效的导带电子俘获剂, 外加氧化剂作为电子受体能提高光催化降解的效果. 实验考察了以卤酸盐KClO3、KBrO3、KIO3为电子受体对光催化反应的影响, 催化剂为180℃、pH值为2反应液中水热2 h制备的BiVO4, 结果如图9所示(电子受体浓度均为0.005 mol/L).
在光催化体系中, 仅加入电子受体而不加入BiVO4催化剂时, 亚甲基蓝的降解率很低, 分别为 4 h 11.2% (KClO3)、0.5 h 13.4% (KBrO3)、2 h 7.6% (KIO3). 仅加入BiVO4, 对亚甲基蓝的降解率达到92.4%时需要4 h (图 6a). 而加入卤酸盐后, 降解速度有不同程度的提高, 以KBrO3作用最为明显, 仅0.5 h亚甲基蓝降解率即可达到98.1%. 这是由于一方面溴酸钾具有良好的接受电子能力(BrO3- + 2H+ + e- →BrO2- +H2O), 可以抑制光生电子和空穴的复合. 另一方面, BrO3-接受电子虽然不直接产生光催化的主要活性氧成分•OH, 但是它可以产生其它的氧化物质, 如BrO2-, HBrO. 这些氧化物质与BrO3-一起直接作为氧化剂参与有机物降解过程, 使得降解速率加快.
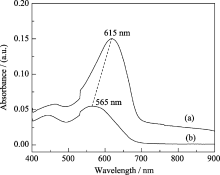
图 10比较了光催化体系中加入KBrO3后对亚甲基蓝紫外-可见吸收光谱的影响. 结果表明, KBrO3不仅加速了亚甲基蓝的降解, 而且对其降解也更彻底. 与不加KBrO3仅以BiVO4降解4 h后的光谱比较, 加入KBrO3仅半小时, 亚甲基蓝溶液的最大吸收峰的强度更低, 且最大吸收峰的位置进一步蓝移, 说明亚甲基蓝的脱甲基过程进行得更为彻底, 不仅在天青C的基础上进一步脱甲基变为硫荃(最大吸收波长602.5 nm), 而且其主体吩噻嗪结构也可能被进一步破坏[ 32].
用水热法在无添加剂条件下制备了不同结构和形貌的BiVO4. 水热温度与反应液pH值对产物有很大影响. 180℃的水热温度和酸性条件有利于单斜相BiVO4的生成, 不同反应液pH条件下得到不同形貌的BiVO4.
所制备的BiVO4在可见光照射下可有效光催化降解亚甲基蓝溶液. 180℃、pH值为2反应液中水热2 h制备的BiVO4具有最好的催化效果. 在光催化反应体系中, 催化剂用量为1.0 g/L, 染液初始浓度为10 mg/L, 电子受体为KBrO3时光催化降解的效果最好.
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|